דלקות פרקים היא מחלה כרונית הפוגעת באיכות החיים של החולה באופן ניכר.
דלקת מפרקים הי תופעה הגורמת לשחיקת הסחוס הנמצא בין המפרקים ולצמיחת בליטות עצם במפרקים.
תסמינים אופיינים לדלקת מפרקים כוללים כאבי מפרקים, קשיות, נפיחות, עייפות ושינויים במראה החיצוני.
על פי ה-CDC דלקת פרקים משפיעה על 24% מהאמריקאים המבוגרים וסה"כ סובלים מהמצב הזה כ-350 מיליון אנשים בכל העולם.
הגורמים העיקריים לדלקות מפרקים
על פי הרפואה דלקת מפרקים יכולה להופיע בעקבות טראומה או חבלה באחד המפרקים, או עקב ביצוע פעולה חוזרת שמפעילה עומס רב על המפרקים. כמו כן, היא יכולה להיגרם כתוצאה משחיקה, ולכן נפוצה במיוחד בקרב קשישים.
במקרים שכיחים פחות, הדלקת נגרמת כתוצאה מבעיות רפואיות אחרות, הפוגעות בחלקים נוספים בגוף, כגון זאבת (לופוס), הפוגעת בכליות, בריאות ובמפרקים, או פסוריאזיס (מחלת עור), שלעתים משפיעה גם על המפרקים.
על פי המדע למזהמים סביבתיים (זיהום אוויר, חומרי הדברה), תרופות הפוגעות במיקרוביום במיוחד אנטיביוטיקה ומזון מעובד ומסוכרר. יש חלק נוסף.
יש 2 סוגים עיקריים של דלקות פרקים:
- דלקת מפרקים ניוונית (OA) היא הצורה הנפוצה יותר של דלקת פרקים. זה מתרחש כאשר הסחוס המגן שמרכך את קצוות העצמות נשחק עם הזמן. למרות שהיא יכולה לפגוע בכל מפרק, ההפרעה פוגעת לרוב במפרקי הידיים, הברכיים, הירכיים ועמוד השדרה. הערכות מדברות על קרוב ל-600 מיליון אבחונים בעולם נכון לנתונים שפורסמו ב-2023.
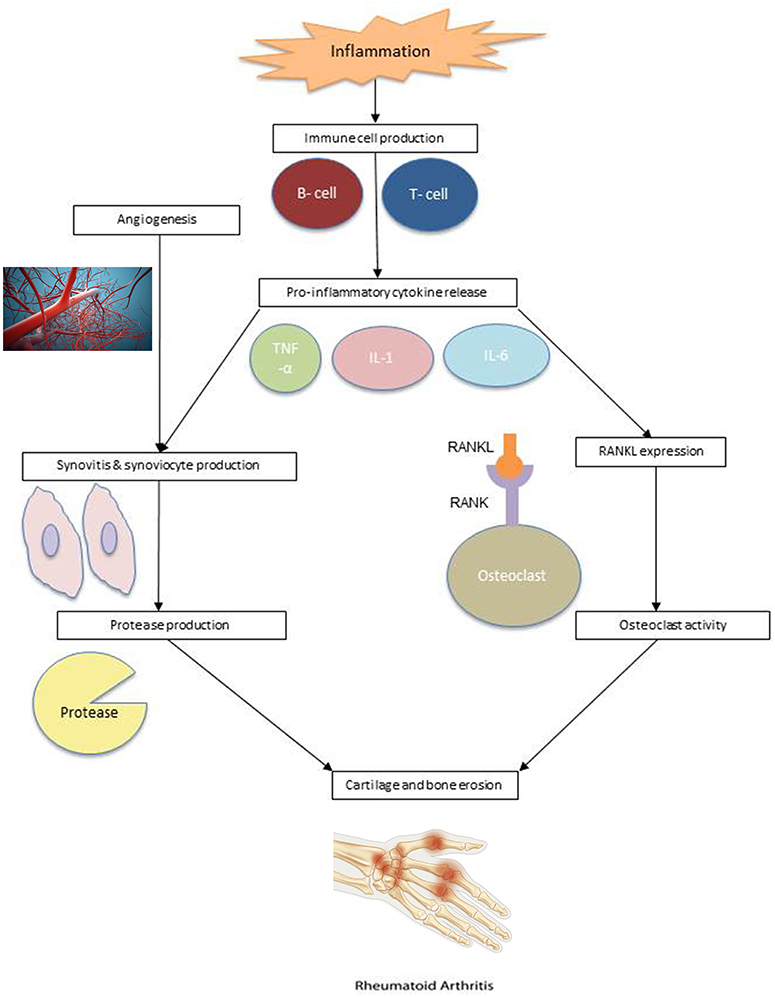
- דלקת מפרקים שגרונית (RA) – הפרעה דלקתית כרונית שיכולה להשפיע על יותר מרק על המפרקים. אצל אנשים מסוימים, המצב מתרחב למערכות נוספות כמו העור, העיניים, הריאות, הלב וכלי הדם.
דלקת מפרקים שגרונית משפיעה על רירית המפרקים וגורמת לנפיחות שעלולה לגרום בסופו של דבר לשחיקת עצם ולעיוות במפרקים.
הטיפול הקונבנציונלי התרופתי
- תרופות אנטי דלקתיות לא-סטרואידליות (NSAIDs): איבופרופן, אספירין, דיקלופנק (וולטרן), פנופרופן – להקלת כאב, נוקשות והפחתת דלקת (לא מאטות התקדמות מחלה).
להן השלכות בריאותיות חמורות (ראו לינקים). - סטרואידים: פרדניזון או סטרואידים במתן תוך-ורידי או בהזרקה למפרק – להפחתת הכאב והדלקת.
- אופיאטים שהם גורם המוות העיקרי עקס התמכרות מתוך התרופות המיועדות לכאבים.
*** תוספת מאי 25
במחקר שפורסם במאי 25 בכתב העת Radiology בהובלת חוקרים מאוניברסיטת UCSF העריכו את הקשר בין זריקות תוך-מפרקיות – הליך רפואי שבו מוזרקת תרופה ישירות לחלל המפרק – לבין התקדמות דלקת מפרקים ניוונית ותוצאות קליניות לאורך תקופה של שנתיים.
נתונים נותחו ממחקר תצפיתי רב-מרכזי, אורכי, של כמעט 5,000 גברים ונשים עם דלקת מפרקים בברך – בחסות המכונים הלאומיים לבריאות – הנמצא כעת בשנת המעקב ה-14 שלו.
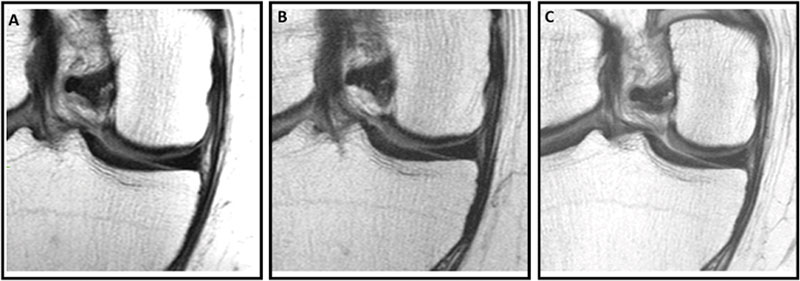
צוות המחקר בחן 70 משתתפים מתוכם 44 הוזרקו קורטיקוסטרואידים, ו-26 חומצה היאלורונית) אחת בברך. המשתתפים הללו עברו MRI של הברך לפני, בזמן ושנתיים לאחר ההזרקה. הם גם העריכו כמה נזק נגרם בחלקים שונים של מפרק הברך לאורך זמן באמצעות Whole-Organ Magnetic Resonance Imaging Score (WORMS). ציונים אלה הושוו לקבוצת ביקורת של 140 אנשים עם מאפיינים דומים שלא קיבלו זריקה כלשהי.
החוקרים מציינים שזהו המחקר הראשון שהשתמש ב-WORMS כדי להעריך את התקדמות דלקת מפרקים ניוונית של הברך לאחר זריקה תוך-מפרקית עם מעקב של שנתיים ושמחקרים קודמים הסתמכו בעיקר על הערכות רנטגן או MRI שדורש עיבוד מיוחד לאחר מכן. לכן שלא כמו אלה, המחקר הנוכחי השתמש בניקוד חצי-כמותי ש"ניתן לבצע בסביבות קליניות ומבודד חולים שקיבלו זריקה אחת בלבד".
המחקר מצא כי זריקת קורטיקוסטרואידים בודדת הובילה לנזק מבני גדול משמעותית במפרק הברך במשך שנתיים בהשוואה לקבוצת הביקורת ולאלו שקיבלו זריקות חומצה היאלורונית שם נצפתה הפחתה של התקדמות הנזק למפרקים ואף נראה שהאטו את הנזק בהשוואה ללפני ההזרקה. החוקרים הסבירו ש"קורטיקוסטרואידים ידועים כמפחיתים דלקת אך גם פוגעים במנגנוני התיקון של הסחוס ויכולים לעכב סינתזת מטריקס – המרכיב העיקרי של הסחוס שנותן את התכונות שלו, כמו גמישות, חוזק וכו'. לכן עם הזמן, הדבר עלול להוביל להחלשת הסחוס ולעלייה ברגישות לנזק, מה שמאיץ את התקדמות דלקת מפרקים ניוונית.
החוקרים מוסיפים ש"ישנן גם עדויות לשינויים בעצם התת-סחוסית ולסיכון לשברים מהזרקות סטרואידים".
החוקרים מקווים שמחקר זה יוביל לשימוש מושכל יותר בזריקות קורטיקוסטרואידים, במיוחד עבור חולים עם דלקת מפרקים ניוונית קלה עד בינונית שעדיין אינם מועמדים לניתוח. הם גם מציעים לבחור בזריקות חומצה היאלורונית בתדירות גבוהה יותר או לשקול אסטרטגיות חלופיות לניהול כאב שאינן מאיצות הידרדרות מבנית.
__ _
_
https://www.rsna.org/news/2025/may/knee-arthritis-made-worse
הקשר למיקרוביום
מיקרוביום המעי – קהילה מגוונת ומורכבת של מיקרואורגניזמים המאכלסים את מערכת העיכול, המורכבת מכ-35,000 מיני חיידקים, ממלא תפקיד קריטי בספיגת חומרים מזינים, שמירה על איזון מטבולי, ויסות מערכת החיסון והפחתת דלקת מערכתית.
*** תוספת נובמבר 24
מחקר שפורסם באוקטובר 24 בכתב העת Annals of the Rheumatic Diseases, בהובלת חוקרים מאוניברסיטת Leeds בין האם שינויים במיקרוביום של המעי יכולים להוביל לפיתוח דלקת מפרקים שגרונית והאם זמן זה יכול לספק חלון הזדמנויות לטיפול מונע.
המחקר מצא שחיידקים הקשורים לדלקת נמצאים במעיים בכמויות גבוהות יותר בערך עשרה חודשים לפני שחולים מפתחים דלקת מפרקים שגרונית קלינית המשפיעה על יותר מחצי מיליון אנשים בבריטניה.
החוקרים מציינים שמחקרים קודמים כבר קישרו בין דלקת מפרקים שגרונית למיקרוביום המעי, אבל המחקר הזה חושף נקודת התערבות אפשרית.
הם מסבירים שחולים בסיכון לדלקת מפרקים שגרונית כבר חווים תסמינים כמו עייפות וכאבי פרקים ומכיוון שאין תרופה ידועה, הם נוטים לחוש לעתים קרובות חוסר תקווה.
המחקר הנוכחי לקח בתחילה נתונים מ-124 אנשים שהיו להם רמות גבוהות של נוגדן (CCP+) שמהווה סמן לפיתוח דלקת מפרקים שגרונית. מתוכם 30 התקדמו לדלקת שגרונית.
מתוכם 19 משתתפים עברו גם דגימה אורכית של 15 חודשים ב-5 נקודות זמם שונות. 5 מתוכם התקדמו לדלקת שגרונית והמחקר הראה שיש להם חוסר יציבות במעיים עם כמויות גבוהות יותר של חיידקים הקשורים לדלקת מפרקים שגרונית, כעשרה חודשים לפני ההתקדמות. ל-14 הנותרים, שמחלתם לא התקדמה, היו כמויות יציבות במידה רבה של חיידקים במעיים. מה שמעיד על כך שיש אפשרות למנוע את התקדמות המחלה.
הטיפולים הפוטנציאליים שהחוקרים רוצים לבדוק בחלון של העשרה חודשים כוללים שינויים בתזונה כמו אכילת יותר סיבים, נטילת פרה-ביוטיקה או פרוביוטיקה ושיפור היגיינת הפה כדי לשמור על הרכב מאוזן של המיקרוביום. המגוון החיידקי של קבוצת הסיכון היה נמוך מהותית מקבוצת הביקורת.
https://www.leeds.ac.uk/main-index/news/article/5683/gut-health-signals-could-transform-arthritis-treatment
*** תוספת אפריל 25
מחקר שפורסם באפריל 25 בכתב העת Frontiers in Nutrition, בחן את הקשר בין מדד התזונה למיקרוביום המעי (DI-GM) לבין הסיכון לדלקת מפרקית ניוונית (OA).
DI-GM הוא מדד חדש המשקף את מגוון מיקרוביום המעי בהקשר של מזונות. כלומר מבטא את הקשר בין מזונות או קבוצות מזון לאופי מיקרוביום המעי.
מדד זה מסוכם במונחים של ראיות להשפעה מועילה, שלילית או ללא השפעה נצפית, על מדדי גיוון חיידקי ( α ו-β), רמות חומצות שומן קצרות שרשרת (בוטיראט, אצטט, פרופיונאט, איזובוטיראט – SCFA) בצואה ושינוי ביחסי המערכות וחיידקים ספציפיים.
כאשר רכיבים מיטיבים כוללים: חומוס, סויה, דגנים מלאים, סיבים תזונתיים, חמוציות, אבוקדו, ברוקולי, מוצרי חלב מותססים, קפה ותה ירוק.
רכיבים שליליים כוללים: דגנים מזוקקים, בשר אדום, בשר מעובד ויותר מ-40% מהאנרגיה היומית משומן רווי וטרנס.
השפעה מיטיבה הוגדרה כעלייה ב:
Faecalibacterium, Bifidobacterium, Lactobacillus, Lactococcus, Parabacteroides, Roseburia,
Eubacterium rectale, Eubacterium hallii, Akkermansia, Prevotella, Prevotella copri, Anaerostipes, Anaerostipes hadrus, Veillonellaceae, Parabacteroides distasonis, Gemmiger, ו- Moraxellaceae .
וירידה ב:
Bacteroides, Bacteroides fragilis, Fusobacteria, Streptococcus, Clostridium, Clostridium symbiosum, Clostridium perfringens, Dialister, Alistipes, Bilophila, Ruminococcus gnavus, Dorea, Actinomyces, Odoribacter, Blautia, Lachnospira, Lachnospiraceae, Sutterella, Enterobacteriaceae, ו- Klebsiella sp.
המדד כולל בתוכו שיטת ניקוד כאשר על כל מזון חיובי שנצרך מעל החציון של משתתפי המחקר מקבלים נקודה. ולהיפך, על כל מזון שלילי שנצרך מתחת לחציון של משתתפי המחקר מקבלים נקודה.
הציונים הללו מחולקים בדרך כלל לקבוצות (לדוגמה: 0-3 נקודות, 4 נקודות, 5 נקודות, ו-6 נקודות ומעלה).
החוקרים מציינים שמדד דלקת-חיסון סיסטמי (SII) הוא סמן ביולוגי הנגזר מספירת תאי דם היקפיים, ומספק השתקפות מקיפה של המצב הדלקתי והחיסוני של הגוף. מחקרים מצביעים על כך ש-SII מוגבר באופן חריג במצבים דלקתיים כרוניים שונים וקשור קשר הדוק לחומרת המחלה ולפרוגנוזה שלה.
החוקרים מוספים ש-OA כרוכה בתגובות דלקתיות מקומיות וסיסטמיות כאחד בפתוגנזה שלה וראיות מצביעות על כך ש-SII מוגבר קשור באופן חיובי לחומרת הכאב ולתפקוד לקוי של המפרקים בחולים עם OA. בנוסף, רמות גבוהות יותר של SII נקשרו באופן משמעותי לחומרה הנצפית ברדיוגרפיה של OA, דבר המצביע על כך ש-SII יכול לשמש כסמן ביולוגי פוטנציאלי להערכת פעילות המחלה והתקדמותה.
הם גם מציינים שמיקרוביום המעי ופרוביוטיקה נמצאו יכולים להפחית את ניוון הסחוס במהלך התפרצויות של OA. ומצד שני שדיסביוזה של המעי עלולה להחריף תגובות דלקתיות תוך-מפרקיות בחולים על ידי פגיעה בשלמות מחסום המעי וקידום שחרור ציטוקינים מעודדי דלקת). לכן לדעתם, לבחינת הקשר בין DI-GM ו-OA, כמו גם לתפקיד המתווך של SII, יש ערך מדעי משמעותי.
החוקרים השתמשנו בנתונים מסקר הבריאות והתזונה הלאומי (NHANES) המשתרע על פני השנים 2007-2018.
OA הוערך באמצעות שאלונים שדווחו על ידי המטופל
נתונים תזונתיים שימשו לחישוב ה-DI-GM.
ניתוחים חד ורב משתנים שימשו להערכת הקשר בין DI-GM ל-OA.
ניתוחים משוקללים שימשו לחקירת הקשר של DI-GM עם SII.
ניתוח נוסף העריך את תפקיד ה-SII.
לאחר אי הכללות של משתתפים: מתחת לגיל 20, חסרים בנתונים ונתונים מבלבלים אחרים, נכללו בסופו של דבר, 15,857 משתתפים בניתוח הסופי.
החוקרים נתנו ציון לכל משתנה חיובי או שלילי ובסוף חילקו את הממצאים ל-4 קבוצות: 0-3; 4; 5 ו- שווה או גבוה מ-6.
הניתוח של הקשר בין DI-GM
נבנו שלושה מודלים, כל אחד מותאם לגורמים מבלבלים פוטנציאליים, ונחשף קשר הפוך בין DI-GM לבין הסיכון ל-OA. כדי להעריך את החוסן של ממצאים אלה, DI-GM חולק לרבעונים. בכל שלושת המודלים נצפה קשר הפוך מתמשך בין DI-GM לבין OA. במודל השלישי המותאם במלואו, הקבוצה עם הציון הגבוה ביותר (DI-GM ≥ 6) הייתה עם סיכון מופחת של 45% לעומת הקבוצה עם הציון הנמוך.
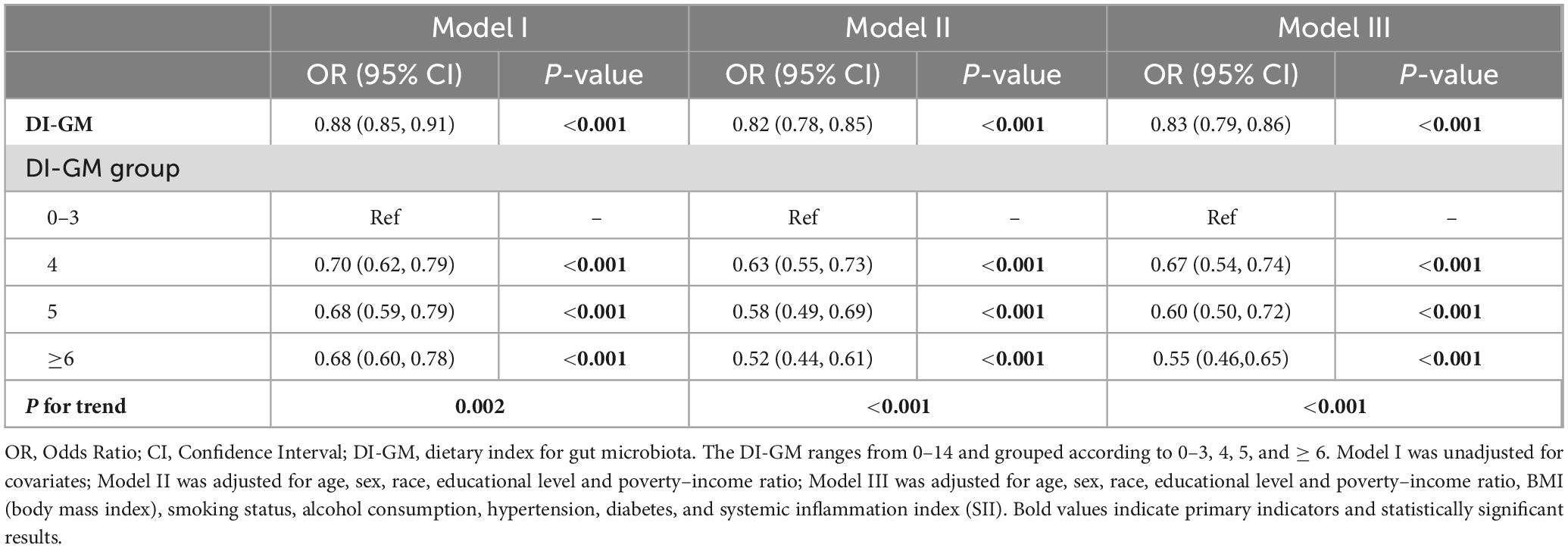
בניתוח הקשר בין DI-GM לבין SII נצפתה קורלציה שלילית בין DI-GM גבוה יותר לבין SII בכל שלושת המודלים. עלייה של נקודה אחת בציון DI-GM קשורה לירידה של 9.2% במדד SII.
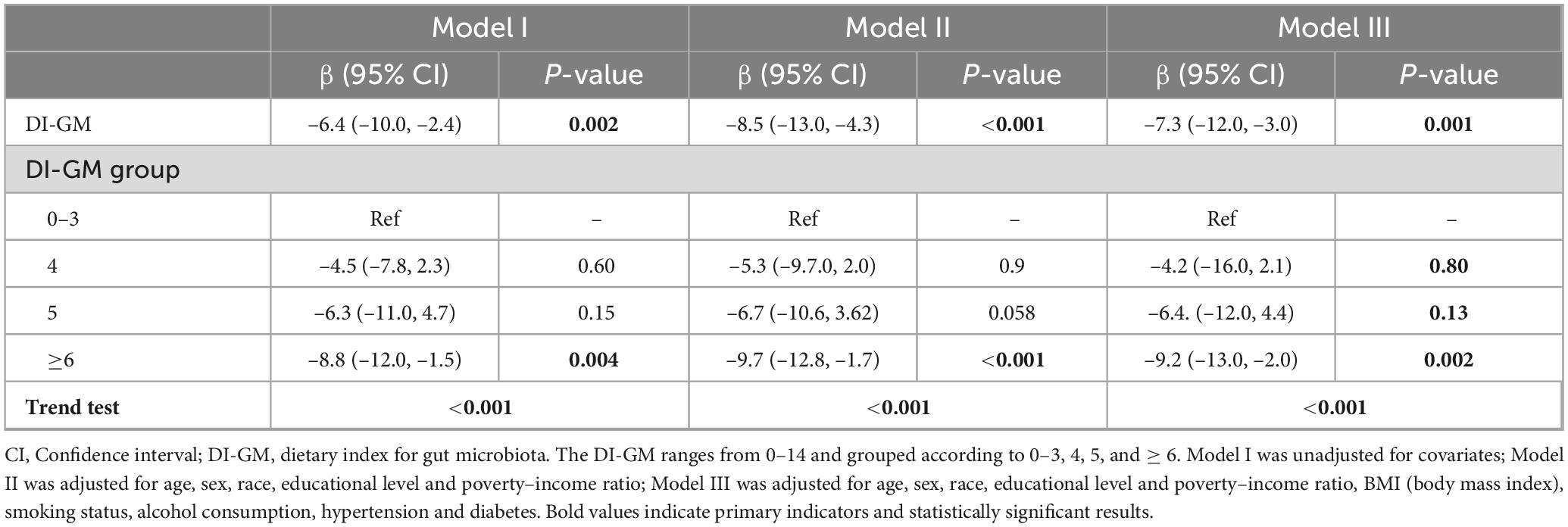
בניתוחי תת-קבוצות לא נמצאו אינטראקציות משמעותיות בין קבוצות המסווגות לפי גיל , מין, גזע/מוצא אתני, רמת השכלה, יחס עוני-הכנסה (PIR), מדד מסת גוף (BMI), יתר לחץ דם, סטטוס עישון וצריכת אלכוהול מה שמצביע על כך שאף אחד מהגורמים הללו לא השפיע באופן משמעותי על הקשר בין DI-GM לבין OA.
המחקר מצביע על כך שציוני DI-GM גבוהים יותר עשויים להפחית את הסיכון ל-OA על ידי ויסות רמות SII. מיקרוביום מעי בריא ומגוון תורם לשמירה על שלמות מחסום רירית המעי. זה, בתורו, מפחית תגובות דלקתיות מערכתיות וממתן דלקת כרונית המעורבת בפתוגנזה של OA.
לכן, סיכמו החוקרים, המחקר מדגיש את הפוטנציאל של התערבויות תזונתיות המתמקדות ב-DI-GM כאסטרטגיה לניהול OA. והנחיות תזונתיות לחולי OA צריכות לתת עדיפות להגדלת הגיוון המיקרוביאלי התזונתי.
החלק של תזונה (מבוססת צומח):
- מחקר שפורסם בנובמבר 17 בכתב העת Frontiers in Nutrition מציע לשלב סיבים תזונתיים ספציפיים, ירקות, פירות ותבלינים, כמו גם סילוק רכיבים הגורמים לדלקת ולנזק. כלומר לעבור לדיאטות כמו ים-תיכונית, טבעונית.
על פי החוקרים המחקר הנוכחי מספק הערכה יסודית מאוד של הידע המדעי הנוכחי תוך דיווח רק על התערבויות תזונתיות ומזונות ספציפיים שמראים בבירור השפעות מוכחות לטווח ארוך.
המזונות שנמצאו מפחיתים את ההתקדמות והתסמינים של דלקת מפרקים שגרונית נעים מפירות כמו שזיפים מיובשים, אוכמניות ורימונים, ועד לדגנים מלאים, צמחי התבלין ג'ינג'ר וכורכום, כמו גם חומצות שומן (אומגה 3) ותה. שיכולים לספק מגוון השפעות מועילות, כגון הפחתת ציטוקינים דלקתיים, הפחתת נוקשות וכאבי מפרקים, כמו גם הורדת עקה חמצונית והיכולת לנטרל או לנקות כימיקלים מזיקים.
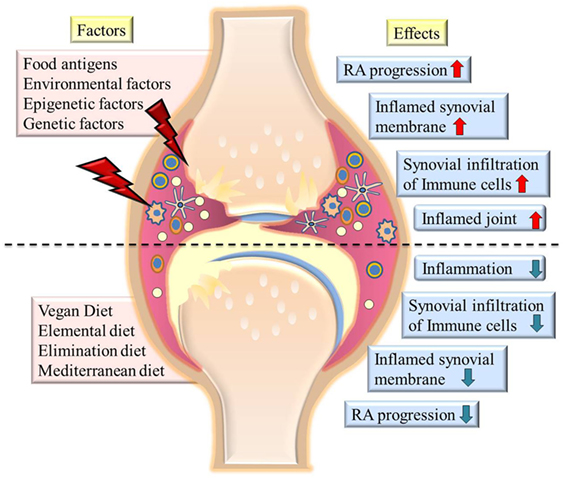
- במחקר שפורסם בספטמבר 2019 בג'ורנל הרפואי Frontiers In Nutrition מראים את הקשר של תזונה על RA.
מספר מחקרים הראו כי כאבי מפרקים ותסמיני RA אחרים עשויים להשתנות על ידי גורמים תזונתיים. משקל גוף מופרז ודיאטות הכוללות מוצרים מן החי (למשל, חלב, בשר אדום) נראו מחמירים את תסמיני RA, ככל הנראה בשל ההשפעות הפרו-דלקתיות שלהם.
מחקרים מראים שאצל אנשים הצורכים יותר מזונות מהחי מדדי החלבון CRP, אינטרלוקין (IL-6) והומוציסטאין נמצאים ברמות גבוהות יותר ולחילופין אצל אנשים עם דיאטות עשירות בירקות, פירות וסיבים (טבעונים וצמחונים) מדדים אלה נמצאים תקינים, כמו גם BMI נמוך יותר – תכונות אנטי דלקתיות המסייעות בהפחתת כאב ודלקת.
מחקרים מראים גם שככל שמשתתפים צורכים רמות גבוהות יותר של בשר אדום מציגים סיכון גבוה יותר לפוליארתריטיס דלקתי בהשוואה למשתתפים עם צריכת בשר וחלבון נמוכה.
אחד הדברים הבולטים שמבדיל בין תזונה מבוססת צומח לתזונה מבוססת חיות הוא כמות הסיבים התזונתיים (מסיסים ושאינם מסיסים) שנמצאים משפרים את מגוון חיידקי המעיים ותפקודם. בין היתר על ידי ייצור חומצות שומן קצרות שרשרת (SCFAs) להן תכונות נוגדות דלקת. כמו כן בריאות החיידקים שומרת על מחסום מעי שלם על ידי הזנת הקולונוציטים מייצרי הריר. ובכך נמנעת חדירה של רכיבים מעודדי דלקת למחזור הדם ולמפרקים.
- *** תוספת אפריל 24
מחקר שפורסם באפריל 24 בכתב העת Medicine בהובלת מדענים מהאוניברסיטה Southern Medical שבסין. החוקרים השתמשו ברנדומיזציה מנדליאנית – שיטה המשתמשת בשונות מדידה בגנים (פולימורפיזם) כדי לבחון את ההשפעה הסיבתית של חשיפה על תוצאה, כלומר כיצד גנים ספציפיים לדלקות מפרקים מגיבים לפירות (יבשים).
הניתוח הראה קשר סיבתי פוטנציאלי בין צריכת פירות יבשים לבין סיכון מופחת לאוסטאוארתריטיס. כלומר זה מצביע על כך שהתערבויות תזונתיות עשויות להיות שימושיות במניעה וניהול של סיבוכים הקשורים לאוסטאוארתריטיס.
החוקרים מציינים שהתרכובות הביו-אקטיביות הקיימות בפירות יבשים, הכוללות בין היתר פנולים, פלבנואידים, קרוטנואידים, פרואנטוציאנידינים, סטילבנים (תרכובות פנוליות) וופיטואסטרוגנים, ידועות כמפחיתות עקה חמצונית ודלקת ומונעות נזק לכונדרוציטים (תאי סחוס).
החוקרים מסבירים שפירות יבשים מכילים כמויות גבוהות פי 3-5 של מינרלים וויטמינים מאשר פירות טריים. חומרים מזינים אלה יכולים להפחית ביעילות את הסיכון לאוסטאוארתריטיס על ידי שיפור חילוף החומרים בגוף. כמו כן הם מציגים עדויות עדכניות שמצביעות על כך שפירות יבשים יכולים להקל על תסמינים הקשורים לאוסטאוארתריטיס על ידי וויסות של מיקרוביום המעי ומטבוליטים ששהם מייצרים. - *** תוספת יוני 24
ניסוי שנמשך 16 שבועות חקר את ההשפעות של התערבות רב-תחומית באורח חיים באנשים עם RA, בהשוואה לטיפול רגיל. ההתערבות התבססה על תזונה מלאה וצמחית – לצד פעילות גופנית וניהול מתחים. ממצאי המחקר פורסמו ביוני 24 בכתב העת Annals of the Rheumatic Diseases.
החוקרים מציינים שדיווחים קודמים כבר הראו שהתערבות זו הפחיתה משמעותית את ציון מחלות מפרקים (DAS28) בהשוואה לטיפול רגיל בלבד[1][2]. כדי להרחיב על כך, הם רצו לקבוע את היעילות ארוכת הטווח של ההתערבות, בהתייחס למחלה לאחר תקופה של שנתיים.
הניסוי המקורי אם כן היה 16 שבועות לאחריו, גם קבוצת הביקורת קיבלה את ההתערבות, והמשתתפים היו במעקב במשך שנתיים עם ביקורים דו-שנתיים ושישה סמינרים מקוונים לקידום הדבקות. אנשים עם ציון נמוך מ-2.6 במחשבון DAS28 קיבלו גם פרוטוקול כגישה מוצעת לנסות להפחית את התרופות האנטי-ראומטיות שלהם – וכל שינוי בטיפול תועד.
בסך הכל, 62% מהמסיימים את הניסוי המקורי השלימו גם את המעקב של שנתיים. אלו שהפסיקו לרוב ציינו כי הסיבה לכך היא שהם היו עסוקים מדי, בלתי נגישים או לא נתנו אישור לשנה השנייה של ההרחבה.
התוצאות ארוכות הטווח הראו שהשיפור ב-DAS28 נשמר במשך שנתיים לאחר השלמת ההתערבות והיה נמוך משמעותית בהשוואה לבסיס. גם מבחן Tender joint count ומרכיבי הבריאות הכלליים השתפרו באופן משמעותי. התוצאות היו דומות באנשים שהשלימו את מחקר ההרחבה בן השנתיים לעומת אלו שהפסיקו את הטיפול בטרם עת.
מתוך 39 המשתתפים שהשלימו את המעקב והשתמשו בתרופות אנטי-ראומטיות, 44% הצליחו להפחית או להפסיק, ל-26% היה שימוש יציב, ו-31% קיבלו טיפול תרופתי מוגבר. מבין אלו עם טיפול תרופתי יציב או מופחת בהשוואה לקו הבסיס, אצל 65% חל שיפור ב-DAS28.
דברים נוספים שהבחינו בהם לאחר המעקב של שנתיים הכולסטרול HDL עלה וחלבון C-reactive (CRP) נשאר נמוך משמעותית בהשוואה לערכי הבסיס. - *** תוספת אוגוסט 25
החוקרים מציינים שדלקת מפרקים שגרונית (RA) משפיעה על כ-1% מהאוכלוסייה העולמית ושכיחה יותר בנשים בגילאי 20-45. ובעוד שגורמים גנטיים עשויים להגביר את הסיכון למחלה, החוקרים טוענים שגורמים סביבתיים, ובעיקר תזונה, יכולים להשפיע על התפתחותה. המחקר הנוכחי בוחן את הפוטנציאל של דפוסים תזונתיים אנטי-דלקתיים, כמו התזונה הים-תיכונית, כחלק מהטיפול בחולי RA.
החוקרים בחנו את ההשפעה של דפוסים תזונתיים בעלי תכונות אנטי-דלקתיות, תוך התמקדות בתזונה הים-תיכונית תוך התייחסיות לרכיביה העיקריים, כגון ויטמינים, מינרלים, חומצות שומן רב בלתי רוויות ואומגה 3, ומסבירים את מנגנוני הפעולה הביוכימיים שלהם על תהליכי דלקת וכאב. הם מדגישים את יכולת התזונה להפחית יצירת רדיקלים חופשיים ולהוריד את רמות הציטוקינים, שהם מולקולות מעודדות דלקת. המחקר מציג כי דפוסים תזונתיים אלו עשויים להפחית את הסיכון למחלה, להפחית סיבוכים ולשפר את התסמינים הקליניים. המחקר גם מציין כי באמצעות הפחתת מדדי דלקת והגברת מנגנונים נוגדי חמצון, התזונה הים-תיכונית יכולה להפחית את רמת פעילות המחלה, לשפר ממצאים קליניים וביוכימיים ולשפר את איכות החיים של החולים. אמנם הם גם מדגישים שחשוב לשקול את השונות של תגובות אינדיבידואליות להתערבויות תזונתיות, שכן היו (ותמיד יש) תוצאות סותרות באוכלוסיות גדולות) ולא כולם מקבלים את כל מרכיבי התזונה באותה צורה. החוקרים מסכמים כי שילוב אסטרטגיות תזונתיות בעלות תכונות אנטי-דלקתיות יכול להיות תוספת חשובה לטיפול המקובל ב-RA ולשפר את איכות החיים של החולים. המאמר מדגיש את החשיבות של גורמים סביבתיים כמו תזונה בניהול מחלה דלקתית כרונית. - *** תוספת אוקטובר 25
סקירת עומק רחבת היקף שפורסמה באוקטובר 25 בכתב העת Frontiers in Nutrition מאששת באופן נחרץ את המגמה המדעית המודרנית: הטיפול בדלקת מפרקים ניוונית (OA) חייב לכלול אסטרטגיה תזונתית מובנית המכוונת לטפל בשורשי המחלה, מעבר להקלה על כאב בלבד. המחקר נערך במטרה לבחון באופן דיאלקטי ומאוזן את המנגנונים הפתולוגיים החדשים המקשרים תזונה ל-OA – כלומר, ציר מטבוליזם-דלקת-עקה חמצונית – ולאחד את העדויות הקליניות לכדי תוכנית טיפול הדרגתית.
החוקרים הגיעו למסקנה כי OA אינה מחלה שחיקתית-מכנית גרידא, אלא הפרעה מטבולית-דלקתית כרונית. הפתולוגיה מתחילה כתוצאה מסיכון יתר של השמנה ותסמונת מטבולית המעודדים דלקת מערכתית. זו בתורה מפעילה עקה חמצונית, הגורמת לייצור מוגבר של רדיקלים חופשיים (ROS) הפוגעים במיטוכונדריה של תאי הסחוס (כונדרוציטים) ומחבלים ביכולתם לייצר קולגן.
המחקר בחן את היתרונות הקליניים של רכיבי תזונה מרכזיים, תוך חלוקתם לתחומי פעולה מרכזיים:- נוגדי חמצון ודלקת: נמצא שחומצות שומן אומגה-3 (EPA ו-DHA) ופוליפנולים הם הרכיבים בעלי הפעילות האנטי-דלקתית העוצמתית ביותר, המסוגלים לדכא את מסלול הדלקת המרכזי (NF-κB). אומגה-3, הראתה עקביות בשיפור כאב ודלקת סינוביאלית. בנוסף, המחקר הדגיש את חשיבותם של נוגדי חמצון וויטמינים חיוניים כגון ויטמין C (קריטי לסינתזת קולגן), ויטמין E, סלניום ואבץ, התומכים בהגנה מפני עקה חמצונית בסחוס. ההשפעה הסינרגיסטית של תבלינים וצמחים כגון ג'ינג'ר, כורכום, שום וטימין, העשירים בתרכובות פעילות וגופריתיות (סולפור), נמצאה כמפחיתה דלקת מערכתית.
- תמיכה מבנית במפרקים: רכיבים אלו מספקים חומרי גלם וגירוי לתיקון הסחוס. פפטידי קולגן (במיוחד סוג II), גלוקוזאמין וכונדרואיטין, וחומצה היאלורונית (HA) הוכחו כתומכים סימפטומטיים. הודגש כי גלוקוזאמין וכונדרואיטין יעילים במיוחד במקרים של כאב בינוני עד חמור.
החשיבות של ויטמין D וסידן אושרה לשמירה על הומיאוסטזיס של עצם-סחוס, עם המלצה לשמור על רמות ויטמין D מעל 30 ng/mL. - תמיכה במיקרוביום: החשיבות של ציר המעי-מפרק (Gut-Joint Axis) אושרה, כאשר פרוביוטיקה (בזנים ספציפיים, כגון Lactobacillus casei Shirota) הראתה שיפור בציון הכאב (WOMAC) ובהפחתת הדלקת המערכתית (hs-CRP) על ידי שיקום מחסום המעי.
- המחקר הציב את הדיאטה הים-תיכונית (MD) כדפוס התזונה הבסיסי והמועדף לכל חולי ה-OA, בשל הרכבה האנטי-דלקתי – עשיר בפוליפנולים (שמן זית), אומגה-3, סיבים ונוגדי חמצון.
החוקרים מדגישים מעבר לתוספים ספציפיים על אסטרטגיה תזונתית מותאמת אישית לטיפול במצבים נלווים:- סוכרת: יש לתת עדיפות לבקרת סוכר קפדנית באמצעות דיאטה עם אינדקס גליקמי נמוך (Low GI), והגבלה של פחמימות מזוקקות כדי למנוע הצטברות AGEs (תוצרי גילוקוז מתקדם) הפוגעים בסחוס.
- גיל המעבר: מומלץ על תמיכה מוגברת בסידן, ויטמין D וכן ויטמין K2 (המכוון את הסידן לעצמות במקום לרקמות רכות) כדי לטפל באיזון העצם המופרע כתוצאה מירידה באסטרוגן.
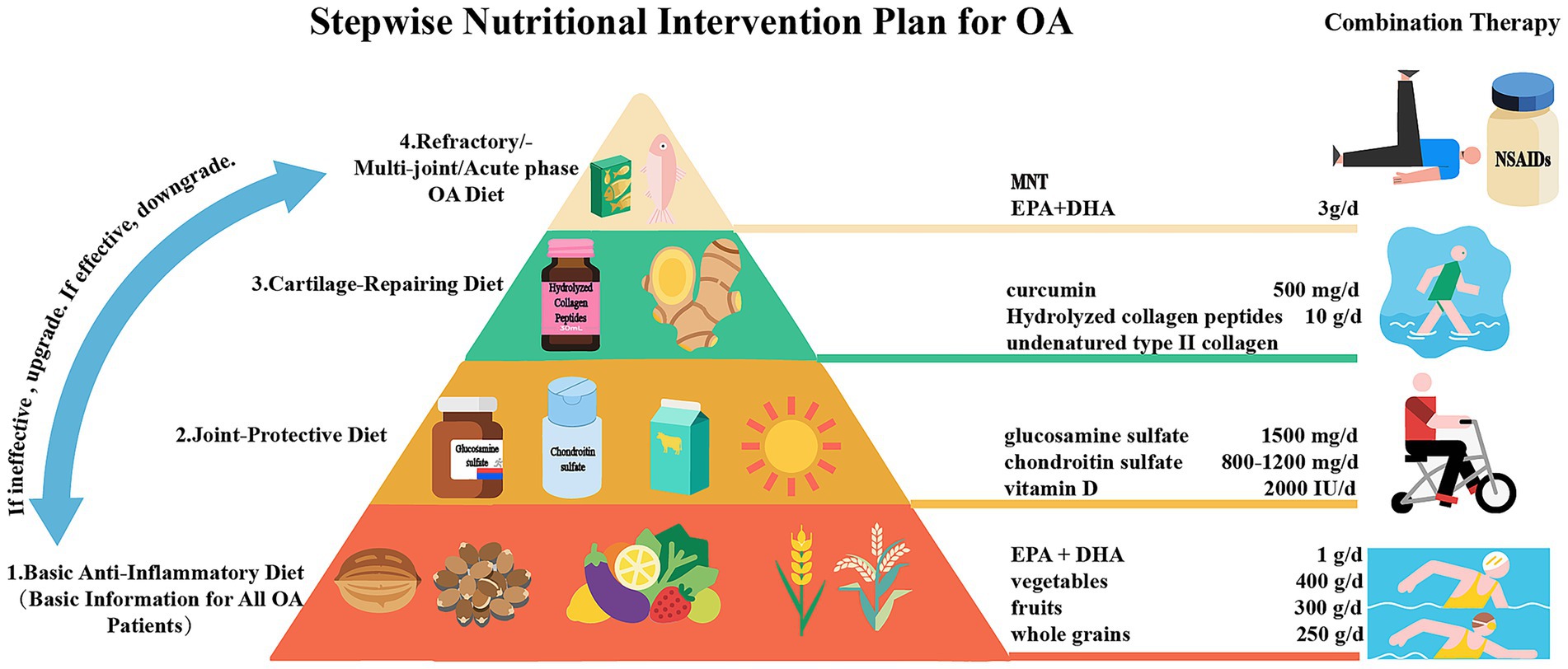
- החוקרים סיכמו את ממצאיהם בתכנית התערבות מדורגת ב-4 שלבים (שלושה חודשים כל אחד), תוך ניטור מתמיד של יעילות הטיפול הקליני.
המחקר מעניק אישור קליני חזק ומציג תמונה הוליסטית של הטיפול התזונתי ב-OA. הוא מאשר את הצורך להפוך את הטיפול התזונתי לפרוטוקול טיפול קו-ראשון ל-OA קלה עד בינונית, המשתלב במודל רב-תחומי, במטרה לדחות או להימנע מניתוחים פולשניים ותלות מוגברת בתרופות. ההמלצות המדויקות לגבי מינונים ושילובים מאפשרות התאמה אישית אפקטיבית של הטיפול.
החלק של שומנים וחומצות שומן:
*** תוספת פברואר 26 – חומצות שומן בדם ואוסטיאוארתריטיס (OA)
מחקר שפורסם בפברואר 26 בכתב העת Cambridge University Press, שופך אור חדש על הקשר הסיבתי שבין פרופיל השומנים בדם לבין הסיכון לשחיקת סחוס ודלקת מפרקים ניוונית (OA). החוקרים השתמשו במתודולוגיה משולבת של ניתוח פנוטיפי (תצפיתי) יחד עם רנדומיזציה מנדליאנית (שיטה המשתמשת בשונות גנטית להוכחת סיבתיות), תוך הסתמכות על מאגרי נתונים ענקיים הכוללים מעל 826,000 נבדקים. הממצאים הצביעו על כך שחומצות שומן רוויות (ללא ציון המקור התזונתי) עשויות להוות גורם סיכון, אך ניתוח המנה-תגובה (RCS) הראה כי הסיכון הופך למובהק רק בצריכת יתר.
לעומת זאת, חומצות שומן חד-בלתי רוויות (MUFA) וחומצות שומן רב-בלתי רוויות (PUFA) זוהו כגורמים מגינים מובהקים ועקביים הרבה יותר, בעלי השפעה סיבתית ישירה על הפחתת הסיכון ל-OA: עבור כל עלייה של סטיית תקן אחת ברמתן בדם, נרשמה ירידה בסיכון הנעה בין 5-6%, בעוד שבניתוח הגנטי הרב-משתני (MVMR) רמות גבוהות של PUFA הפחיתו את הסיכון בשיעור משמעותי של עד 18%, ורמות גבוהות של MUFA בשיעור של עד 11%.
ניתוח גנטי מעמיק חשף 68 מיקומים גנטיים משותפים לשומנים ולדלקת מפרקים, אשר מעורבים במסלולים ביולוגיים של מטבוליזם של ליפופרוטאינים (חלבוני הובלת שומן), תגובה חיסונית וויסות דלקתי. המסקנה הקלינית של החוקרים היא שרמות גבוהות של שומנים בלתי רוויים בדם אינן רק סמן לבריאות, אלא הן פועלות באופן אקטיבי לדיכוי דלקת ולשמירה על שלמות המפרק.
מחקר זה מהווה נדבך קריטי המאחד את הראיות שהוצגו לאורך המאמר, במיוחד בקשר לציר המעי-מפרק (Gut-Joint Axis) והשפעת התזונה הים-תיכונית. בעוד שמחקרים קודמים הדגישו את החשיבות של ויטמינים ופוליפנולים, המחקר הנוכחי מוכיח כי לסוג השומן עצמו יש תפקיד מכריע ברמה הגנטית והמולקולרית. האישור הסיבתי לכך ש-MUFA (הנמצאת בשפע בשמן זית ואבוקדו) ו-PUFA (אומגה 3) מגינות על הסחוס, מחזק את ההמלצה לעבור לתזונה מבוססת צומח המוגבלת בשומן רווי מהחי. הממצאים על המעורבות של מערכת החיסון וויסות הדלקת דרך מטבוליזם השומנים מסבירים מדוע שינוי תזונתי אינו רק אמצעי להפחתת משקל, אלא התערבות ביולוגית ישירה המדכאת את העקה החמצונית ואת הפגיעה המבנית בכונדרוציטים (תאי הסחוס)..
- חומצות שומן מסוג אומגה 3
- מחקר סקירה ממאי 24 בכתב העת Nutrientsמציג מחקרים שמראים באופן עקבי כי אומגה 3 (PUFAs) מפחיתים את פירוק הסחוס ואת רמות הסמנים הביולוגיים הדלקתיים, ובכך מפחיתים את התקדמות OA. אומגה 3 מספק גם יתרונות עקיפים על ידי שיפור התאוששות רקמת השריר לאחר פעילות גופנית.
- *** תוספת יולי 25: אומגה 3 ורפואת אורתופדיה
סקירה נרטיבית מקיפה שפורסמה ביולי 25 בכתב העת Cambridge University Press, סיכמה את התקדמות המחקר והיישומים הפוטנציאליים של חומצות שומן אומגה 3 (n-3 PUFAs) בתחום האורתופדיה. הסקירה מדגישה כי אומגה 3, הכוללות ALA, EPA ו-DHA, קריטיות לבריאות אך חסרות לעיתים קרובות בתזונה המודרנית, מה שמגביר את העניין בתוספים. בתחום האורתופדיה, אומגה 3 מפעילה השפעות מיטיבות באמצעות מספר מנגנונים מרכזיים:
וויסות תגובות דלקתיות: מפחיתה את התגובה הדלקתית המעורבת במצבי פרקים.
שיפור תיקון סחוס: תורמת לשיקום ותחזוקת הסחוס במפרקים.
וויסות מטבוליזם העצם: מסייעת בשמירה על בריאות וחוזק העצמות.
החוקרים מצביעים על פוטנציאל טיפולי משמעותי של אומגה 3 במגוון רחב של מצבים אורתופדיים, ביניהם: אוסטאוארתריטיס (OA), דלקת מפרקים שגרונית (RA), גאוט, אוסטאופורוזיס (OP), שברים, סרקופניה (איבוד מסת שריר) ומחלות ניווניות של עמוד השדרה. הסקירה מדגישה את החשיבות ההולכת וגוברת של אומגה 3 כאסטרטגיה תזונתית משלימה לטיפול ומניעה של מחלות אלו.
לחלק של הפרקטיקה! מה עושים עכשיו ואיך מיישמים את כל הידע הזה.
🧰 ארגז הכלים המעשי, 🗓️ תוכניות פעולה הדרגתיות ליישום הרגלים קריטיים.
🛒 רשימות קניות ממוקדות וטבלאות רכיבים, 👨🍳 מתכונים קלים ומדויקים.
💡 הנחיות יישום (מה זה אומר בפועל). 🔬 הרחבות, נספחים, 🚨 תוספים ודיוקים.
🌟המודולים מסודרים בטבלה לפי נושאים נחקרים 🌟
👈 מוזמנים לפנות אלי באופן פרטי לווטסאפ (0544-606696).👉
🤝 ולהכיר את הקבוצה: "לצאת מעדר הרגיל – הפרקטיקה"
דברים ספציפיים למניעה וטיפול
- צמחי תבלין/מרפא ומזונות על:
- רכיבי תזונה
- פרוביוטיקה [1][2][3][4][5][6][7], גאוט [9][10].
- פעילות גופנית.
- כאבים – תרופות מול תוספי מזון.
היי לך.. אני משקיע שעות רבות כל יום באיתור ותרגום מאמרים כדי לספק לכולם את המידע העדכני ביותר, לבריאות טובה בדרך הטבע. וכדי שאוכל להמשיך לספק את המידע ולתחזק את האתר. כל תרומה, גדולה או קטנה תהיה לעזר רב. לתרומה נוחה ופשוטה דרך Pay Pal.
כדי להתעדכן ראשונים מוזמנים להזין דוא"ל למטה





כתיבת תגובה