לתזונה חלק עיקרי בעיצוב המיקרוביום של המעי, שמזוהה כאחד מכמה גורמים מרכזיים פוטנציאליים הממחישים את ההשפעה התזונתית על בריאות ומחלות (מערכת חיסון; מחלות מטבוליות; מערכת העצבים ההיקפית, המוח וגוף-נפש ומחלות לב וכלי דם).
מבוא וסקירה על חומצות שומן קצרות שרשרת (SCFAs)
SCFAs הם מטבוליטים המיוצרים על ידי חיידקים ספציפיים של מיקרוביוטת המעי האנושית, וייצורם מושפע ממזונות ספציפיים או תוספי מזון, בעיקר סיבים תזונתיים, פוליסכרידים בלתי ניתנים לעיכול – פרהביוטיקה. הם ממלאים תפקיד רגולטורי בשיפור בריאות המעיים על ידי שיפור שלמות מחסום המעי, ייצור ריר ושחרור סרוטונין.
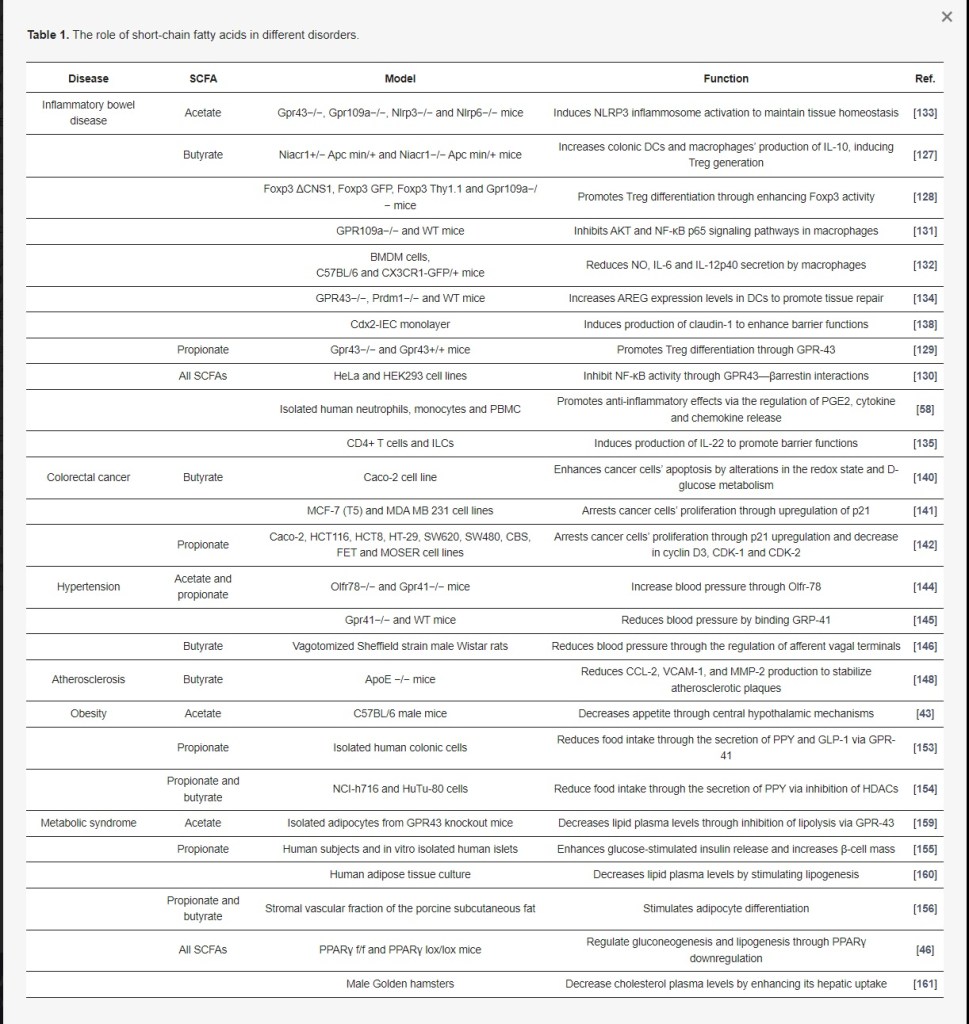
מחסור שלהן נמצא מעורב בפתוגנזה של מספר הפרעות, כולל מחלות מעי דלקתיות, סרטן המעי הגס והחלחולת והפרעות קרדיומטבוליות.
מחקרי התערבות אנושיים הראו ששילוב תזונה מועשרת בסיבים בשגרת היום שלנו יכולה לשפר משמעותית את הרכב המיקרוביוטה של המעיים, וכתוצאה מכך לעלייה בייצור SCFAs בצואה או בדגימות דם. כלומר ה-SCFAs הם חוליה נוספת המסבירה את התועלת של המיקרוביום וסיבים תזונתיים.
ה-SCFAs המוכרים והנחקרים ביותר: בוטיראט, פרופיונט ואצטט
סקירה שפורסמה במאי 23 בכתב העת Nutrients מספקת סקירה כללית של התפקידים והתפקודים של SCFAs, ושל חיידקים המייצרים אותם. כמו כן את הגישות הטיפוליות הפוטנציאליות להגברת רמות ה-SCFAs במעיים האנושיים לטיפול במחלות שונות.
חלבונים נשאים (טרנספורטרים) של SCFA המצויים על משטח האפיתל של המעי הגס מתווכים את ההשפעות של SCFA על המעיים.
להלן חלק מהתפקודים שמצויינים במאמר הקשורים לחומצות השומן הקצרות:
- SCFAs מפחיתים את החדירות ומגבירים את השלמות של מחסום המעי. בוטיראט, למשל, מגביר את הריכוזים של חלבונים מסוימים (tight junction proteins). בוטיראט גם מחזק את שכבת ריר האפיתל של המעי על ידי העלאת ביטוי מוצינים (תאים המייצרים ריר), מווסת רמות עקה חמצונית, מפחית נזקי DNA הנגרמים על ידי מי חמצן, מפחית ייצור ROS, משקם רמות גלוטתיון.
- SCFAs מגבירים את ספירת תאי ה-T הרגולטוריים (Treg) ומפחיתים את רמות הדלקת במעי על ידי הורדת פעילות (NF-κB) ושחרור ציטוקינים רלונטיים.
- SCFAs גם מעוררים התמיינות תאית ו/או תהליך אפופטוזיס כדי למנוע סרטן.
- SCFAs יכולים גם לווסת את הגלוקוניאוגנזה (הפקת סוכר שלא מפחמימה) של המעי המושרה על ידי המוח.
- SCFAs הוכחו גם כמעכבים את פעילות היסטון (HDAC) וכתוצאה מכך, עשויים להשפיע על הפרעות נוירופסיכיאטריות כגון מחלת אלצהיימר, סכיזופרניה ודיכאון.
- SCFAs מווסתים דלקת נוירו-מערכתית על ידי אפנון מבנה ותפקוד תאי מיקרוגליה, כמו גם תפקודים רגשיים וקוגניטיביים.
- SCFAs עשויים גם להשפיע על שלמות מחסום המוח על ידי ייצור אנזימטי של טריפטופן הידרוקסילאז, ובכך להגביר את סינתזת הסרוטונין.
- SCFAs כגון אצטט מורידים את התיאבון על ידי העלאת רמות הורמוני השובע.
- פרופיונאט מוריד את הגלוקוניאוגנזה בכבד.
- בוטיראט ואצטט מעלים את רמות הלפטין שמשתתף במנגנון השובע ומפחית את המשקל ורמות הטריגליצרידים.
- פרופיונאט ובוטיראט מורידים את רמות לחץ הדם על ידי הרחבת כלי דם ומונעים פקקת.
- SCFAs משפרים את ההומאוסטזיס של גלוקוז באמצעות השפעות מווסתות של קולטן גמא (PPARγ).
תפקיד ה-SCFAs באספקת אנרגיה לגוף
*** תוספת יולי 25
עד כה, התמקדנו בתפקידים הרבים והמגוונים של חומצות השומן קצרות השרשרת (SCFAs) בוויסות תהליכים פיזיולוגיים, הפחתת דלקות וחיזוק מחסום המעי. אולם, מעבר לתפקידיהם הרגולטוריים, ה-SCFAs ממלאים תפקיד קריטי ומהותי גם באספקת אנרגיה לגוף המארח. הם נוצרים בתהליך תסיסה אנאירובי של פחמימות מורכבות (כגון סיבים תזונתיים ועמילנים עמידים) על ידי חיידקי המעי הגס, ונספגים ביעילות רבה על ידי תאי המעי והגוף כולו, ומשמשים כמקור אנרגיה חשוב, במיוחד עבור תאי המעי עצמם. הבנה מעמיקה של היקף תרומה זו חיונית כדי להבין באופן שלם את האינטראקציה בין המיקרוביום לתזונה ולבריאות.
מחקר שפורסם ביולי 25 בכתב העת Cell מספק לראשונה כימות מדויק ועדכני של היקף תוצרי התסיסה הללו ותרומתם האנרגטית לגוף האדם. צוות החוקרים בכיר פיתח גישה חדשנית ומשולבת כדי להעריך את זרימת המטבוליטים האלה במעי האנושי, תוך התגברות על מגבלות של שיטות מדידה קודמות (שסיפקו רק "תמונות בזק" ולא זרם כולל).
כימות תוצרי התסיסה חושף את היקף תרומתם האנרגטית המשמעותית, אך מהי המשמעות הפרקטית של "אספקת אנרגיה" זו עבור הגוף? ה-SCFAs אינם רק מולקולות איתות חשובות; הם משמשים גם כ"דלק" איכותי ומהיר זמין לרקמות רבות. לדוגמה תאי המעי הגס (קולונוציטים) מסתמכים במידה רבה על בוטיראט כמקור האנרגיה העיקרי שלהם, מה שחיוני לשמירה על שלמות וחוזק מחסום המעי. אצטט ופרופיונאט נספגים ומועברים לזרם הדם, שם הם יכולים לשמש מקור אנרגיה עבור הכבד, השרירים ורקמות אחרות.
מעבר לאספקת אנרגיה ישירה, מחקרים מצביעים על כך ש-SCFAs, במיוחד בוטיראט, משפרים באופן פעיל את תפקוד המיטוכונדריה – "תחנות הכוח" של התא. הם מסייעים בהגברת יצירת מיטוכונדריה חדשה, משפרים את יעילות ייצור האנרגיה (ATP) בתוכן, ואף תורמים להפחתת עקה חמצונית. תפקוד מיטוכונדריאלי מיטבי מתורגם לחיוניות מוגברת, עמידות טובה יותר למאמץ, שיפור בתפקודים קוגניטיביים ומטבוליים, ותורם לבריאות כללית וארוכת טווח.
החוקרים שילבו שלוש גישות משלימות כדי לקבל הערכות עקביות:
- מדידות מעבדתיות מעמיקות: הם גידלו 22 זני חיידקי מעי נפוצים (המכסים כ-60%-84% מהביומסה החיידקית במעי בריא) בתנאי מעבדה ובדקו באופן שיטתי את קצב צריכת הפחמימות וייצור תוצרי התסיסה (אצטט, פרופיונאט, בוטיראט, לקטט, פורמט, סוקסינאט) לכל יחידת ביומסה חיידקית. הממצאים הראו עקביות רבה גם בתנאי pH שונים ובמגוון מצעי גידול, מה שהעיד על יציבות היחסים המטבוליים.
- ניתוח פיזיולוגי של מערכת העיכול האנושית: הם שילבו נתונים על צריכה תזונתית, עיכול וספיגה, יחד עם נתונים על משקל צואה, כדי להעריך כמה פחמימות זמינות לחיידקים (MACs – Microbiota-Available Carbohydrates) מגיעות למעי הגס, וכמה ביומסה חיידקית מיוצרת ומופרשת.
- נתונים מטגנומיים: נתונים על הרכב המיקרוביום ממאגרים גדולים (כולל כ-18,000 דגימות), כדי להבין את השפעת הרכב החיידקים על ייצור ה-SCFAs.
ממצאי המחקר:
- המחקר מצא כי תוצרי התסיסה מספקים בין 2-5% מדרישות האנרגיה היומיות של בני אדם הצורכים תזונה מערבית טיפוסית. לעומת זאת בתזונה שעשירות יותר בסיבים (כמו אצל קבוצת הציידים-לקטים "הדאזה" בטנזניה), תרומה זו יכולה להגיע עד 10% ואף יותר (כ-1,000-1,500 מ"מול ליום), עם שינויים עונתיים המשקפים את צריכת הפחמימות.
- המחקר הבהיר באופן חד-משמעי כי הגורם העיקרי הקובע את הכמות הכוללת של תוצרי התסיסה הנספגים בגוף הוא כמות וסוג הפחמימות המורכבות הזמינות לחיידקים בתזונה, ולאו דווקא ההרכב הספציפי של חיידקי המעי. כלומר, דיאטה דלה בסיבים תוביל לייצור נמוך יותר של SCFAs, ללא קשר להרכב המיקרוביום.
- המחקר גם מצא כי למעלה מ-90% מהפחמימות המורכבות שמגיעות למעי הגס הופכות לתוצרי תסיסה, ורובן נספגות ישירות על ידי המעי ומשמש את הגוף. כאשר פחות מ-2% מה-SCFAs הללו יוצאים מהגוף בצואה, מה שממחיש את חשיבות הספיגה המקומית שלהם.
- למרות שההרכב הכולל של חיידקי המעי אינו משפיע באופן דרמטי על כמות תוצרי התסיסה הכללית, הוא כן משפיע באופן משמעותי על הפרופורציות של סוגי ה-SCFAs השונים (בוטיראט, פרופיונאט ואצטט). לכל SCFA יש תפקידים ייחודיים בגוף, ולכן שינויים בהרכב המיקרוביום עדיין רלוונטיים להשפעות ספציפיות על הבריאות.
החוקרים מדגישים כי ממצאיהם מהווים אבן דרך בהבנת האינטראקציות המטבוליות בין המיקרוביום למארח. הם קוראים לשלב באופן שיטתי את ציר "תזונה-הרכב מיקרוביום-תוצרי תסיסה" בכל המחקרים העתידיים על בריאות ומחלות הקשורות למיקרוביום.
המחקר מדגיש גם את ההבדלים בין המודלים כאשר תרומת המיקרוביום אצל עכברים גבוהה משמעותית (מעל 21% מהאנרגיה היומית) מאשר בבני אדם (עד 12.1% במקרים של תזונה בריאה עשירה בסיבים). מה שמדגיש את החשיבות של יותר מחקרים בבני אדם.
המחקר גם מחזק את חשיבותה העליונה של התזונה כגורם המרכזי בעיצוב התפוקה המטבולית של המיקרוביום. תזונה דלה בפחמימות זמינות לחיידקים, הנפוצה יותר ויותר בעולם המערבי, מובילה לייצור נמוך יותר של SCFAs, עם השלכות בריאותיות אפשריות.
מחקרים ספציפיים עדכנים ורלוונטיים
- *** תוספת נובמבר 23 – פרה פרו ופוסטביוטיקה למניעה וטיפול באלרגיות.
- *** תוספת ינואר 24 – בריאות קרדיומטבולית
מחקר שפורסם בינואר 24 בכתב העת Nutrients, מציג את חשיבות חומצות שומן קצרות אלה עם בריאות קרדיומטבולית. המחקר התעמק מעבר למדדים אנתרופומטריים (משקל, גובה, BMI, היקפים, הרכב הגוף/ אחוז שריר, אחוז שומן,קפלי עור) והרכב גוף כדי לחקור אינדיקטורים מתקדמים יותר הקשורים ישירות לסיכון קרדיומטבולי, כגון יחס השומן הקרביי לשומן התת עורי (VAT/SAT) ואינדקס צורת הגוף (ABSI) שמציג את היחס בין היקף המותניים (WC) ל-BMI.
החוקרים ערכו בדיקות ביוכימיות למשתתפים: סוכר בצום, אינסולין, כולסטרול, טריגליצרידים ורמות חלבון תגובתי (CRP) בסרום. יתר על כן הצוות העריך את התזונה של כל משתתף כולל: אנרגיה, מאקרו-נוטריינטים וצריכת סיבים תזונתיים.
מטרת המחקר הייתה לנתח את ריכוז הצואה של SCFAs אצל גברים ונשים בריאים שאינם שמנים ואת הקשר של גורמי אורח חיים (תזונה, פעילות גופנית, שינה), ריכוזים של SCFAs צואתיים וסיכון למחלות קרדיומטבוליות. החוקרים מציינים שככל הידוע להם, המחקר הזה הוא בין הבודדים לחקור את הקשר בין אינדיקטורים אלה לבין SCFAs (חומצה אצטית, בוטירית, איזובוטירית, פרופיונית, איזובלרית וחומצה ולרית).
להלן הממצאים העיקריים:- מתאם שלילי בולט בין 6 סוגי ה-SCFA ויחס VAT/SAT, BMI ואחוז שומן בקבוצת נשים. אצל הגברים המתאם היה קשור לפרופיוניות ולבוטירית. נמצא גם קשר שלילי בולט בין חומצה ולארית עם היקף המותניים (WC) ושומן בטני אצל הנשים וקשר חיובי לאחוז המים הכוללים בגוף (TBW) והמסה נטולת השומן. כל אלה, מציינים החוקרים, תומכים בכך שחומצות אצטית, בוטירית וולארית עשויות לסייע במניעת השמנת יתר אצל אנשים בריאים.
- בקבוצת הנשים, הריכוז של חומצות אצטית, פרופיונית ואיזוקפריונית וכן הריכוז הכולל של SCFAs הראו קשר חיובי מובהק עם משך השינה שלהם, כלומר משפיע באופן חיובי על השינה.
- עלייה בצריכת סיבים תזונתיים הובילה לרמות מוגברות של חומצה אצטית, פרופיונית, בוטירית וסך SCFAs בקרב גברים ונשים כאחד. בנוסף, רמות חומצה קפרואית וחומצה ולארית עלו אצל גברים. ניתוח התפלגות האחוזים של SCFAs אישר עוד יותר את המתאם הזה, כלומר, רמות גבוהות משמעותית שלהן אצל אנשים עם צריכת סיבים של ≥25 גרם. דבר זה גם מאשר שמיקרוביום המעי מסנתז SCFAs באמצעות סיבים תזונתיים, ותזונה עשירה בסיבים הכוללת סיבים מסיסים יכולה להגביר את הביוסינתזה של SCFA.
להלן רשימה של חלק מהחיידקים שמייצרים SCFAs:
במיוחד מיני Firmicutes הכוללים Lactobacillaceae, Ruminococcaceae ו- Lachnospiraceae. החיידקים: Actinobacteria, Proteobacteria, Fusobacteria, Roseburia ו-Faecalibacterium prausnitzii יכולים לייצר בוטיראט. חיידקים אלה נמצאים ברמות נמוכות או כלל לא אצל חולי IBD.
- *** תוספת אפריל 25 – סוכרת סוג 1
חוקרים מאוניברסיטת קווינסלנד מצאו ששיפור תפקוד המיקרוביום של המעי עשוי לעכב את הופעת סוכרת מסוג 1 (T1D). ממצאי המחקר פורסמו במרץ 25 בכתב העת nature communications .
במחקר שלהם 21 אנשים עם T1D קיבלו טיפול ביותרפיה פומית המכילה SCFA (אצטט, פרופיונאט ובוטיראט).
החוקרים מציינים שסוכרת מסוג 1 היא מחלה אוטואימונית ויודעים שיש משהו שונה במיקרוביום המעי ובתפקוד מחסום המעי שלדעתם משנה את התגובה החיסונית. הם למדו שאפשר לשנות את המיקרוביום אצל אנשים עם T1D, וכשעשו את זה, הם גם ראו שינויים בתפקוד מחסום המעי. ואז כשבדקו עוד יותר את המיקרוביום על ידי העברתו לעכברים עם נטיה לסוכרת, זה עיכב את הופעתה.
החוקרים מוסיפים שהיו גישות אחרות לשחזור חומצות שומן קצרות שרשרת, כמו מתן חיידקים פרוביוטיים או כמוסות, אבל הן לא ממש עבדו. מה שכן קרה עם תוספת SCFA.
"ממצאים אלה מצביעים על התערבויות של מיקרוביום שיכולות לעצור את סוכרת סוג 1 במסלוליה כדי לעכב, או אפילו למנוע T1D, לתת למטופלים הזדמנות להישאר בריאים יותר לאורך זמן ולהגדיל את תוחלת חייהם". ד"ר Eliana Mariño.
https://www.uq.edu.au/news/article/2025/04/gut-microbiome-could-delay-onset-of-type-1-diabetes
- *** תוספת יוני 25 – בוטיראט – בקרת גליקמיה ותובנות עדכניות
בהמשך לתפקידים הרבים של חומצות השומן קצרות השרשרת (SCFAs) שצוינו לעיל, ובפרט בוטיראט, פורסמה לאחרונה סקירה מקיפה שפורבמה ביוני 25 בכתב העת Nutrition and Metabolism. סקירה זו מתמקדת באופן ספציפי בתרומתו המורכבת של בוטיראט לוויסות רמות הסוכר בדם (בקרת גליקמיה) ומספקת תובנות מעמיקות על מנגנוני פעולתו בבעלי חיים ועדויות מבני אדם.
המאמר מדגיש כיצד בוטיראט, המיוצר על ידי מיקרוביום המעי מסיבים תזונתיים בלתי ניתנים לעיכול, מציג יתרונות משמעותיים בבקרת משקל, הפחתת דלקת ושיפור עמידות לאינסולין. המחקר מציג דרך מחקרים בבעלי חיים ובמודלים של תרבית תאים את המנגנונים המרכזיים:- בקרת משקל: הפחתת תכולת השומן ומשקל הגוף, תוך הגברת השריפה של חומצות השומן למטרת אנרגיה ושיפור סבילות לגלוקוז ורגישות לאינסולין.
- תפקוד שרירי השלד: הפחתת תנגודת לאינסולין על ידי שיפור התפקוד המיטוכונדריאלי, הפעלת מסלולים מטבוליים כמו AMPK ועיכוב אנזים HDACs (היסטון דה-אצטילאזות), המשפרים את ספיגת הגלוקוז לשריר.
- תפקוד רקמת השומן: ויסות מטבוליזם האנרגיה והשומנים בתאי השומן, שיפור רגישות לאינסולין והגברת ייצור חלבונים המעורבים בביוגנזה מיטוכונדריאלית.
- בריאות המעיים והשפעה אנטי-דלקתית: המאמר מחזק את המידע הקיים על יכולת הבוטיראט לשפר את שלמות מחסום המעי, להפחית את חדירות המעי ולדכא תגובות דלקתיות במערכות שונות בגוף (על ידי הפחתת ציטוקינים פרו-דלקתיים ועיכוב NF-κB).
- השפעה על המיקרוביום: בוטיראט משפיע בעקיפין על הרכב ותפקוד מיקרוביוטת המעי עצמה, מה שתורם ליתרונות המטבוליים.
- *** תוספת יולי 25 – חידושים במאבק בדלקת
בהמשך לחשיבותם של חומצות השומן קצרות השרשרת (SCFAs) ומרכיבים נוספים המיוצרים על ידי חיידקי המעי, סקירה שיטתית מקיפה שפורסמה ביולי 25 בכתב העת Nutrients מתמקדת בפוסט-ביוטיקה – קטגוריה חדשנית המציעה יתרונות בריאותיים ללא צורך בחיידקים חיים (בניגוד לפרוביוטיקה). היא כוללת מגוון רחב של מטבוליטים חיידקיים (ביניהם חומצות שומן קצרות שרשרת – SCFAs), חלקי דופן תא, פוליסכרידים חוץ-תאיים, פפטידים ועוד. יתרונה הבולט הוא ביציבותה הגבוהה ובטיחותה המשופרת בהשוואה לפרוביוטיקה חיה, מה שהופך אותה לאלטרנטיבה מבטיחה, במיוחד עבור אוכלוסיות רגישות או בעלי מערכת חיסון מוחלשת.
הסקירה מאשרת כי פוסט-ביוטיקה מפעילה השפעות אנטי-דלקתיות רב-גוניות:
וויסות ביטוי ציטוקינים: הפחתת מולקולות מעודדות דלקת (כמו IL-6 ו-TNF-α).
השפעה על מסלולי איתות תאיים: שינוי פעילותם של מסלולים חיסוניים כמו NF-κB ו-MAPK.
חיזוק שלמות מחסום המעי: שיפור יכולת ההגנה של שכבת התאים המצפה את המעי, ובכך מניעת מעבר חומרים מזיקים לזרם הדם ("מעי דליף").
יזון התגובה החיסונית: ויסות האיזון בין תאי חיסון מסוג Th1/Th2 ו-Treg/Th17, המשמעותי במצבים אוטואימוניים ומחלות מעי דלקתיות.
הפחתת עקה חמצונית: חלק מהפוסט-ביוטיקה מציגה תכונות נוגדות חמצון, התורמות להפחתת נזקים תאיים.
המחקר מצביע על פוטנציאל טיפולי של פוסט-ביוטיקה במגוון רחב של מצבים דלקתיים, כולל: מחלות מעי דלקתיות (IBD); מחלות אוטואימוניות; תסמונת מטבולית (לדוגמה, נתרן בוטיראט שהראה שיפור בבקרת גליקמיה); מחלות כבד וכליות; מצבים הקשורים לדלקת כרונית ודיסביוזיס במעי.
סיכום והמלצות מעשיות לשיפור ייצור SCFAs ובריאות המעי (מהמידע הכולל עד כה): תזונה נבונה ממלאת תפקיד מרכזי בעיצוב המיקרוביום של המעי ובהגברת ייצור חומצות שומן קצרות שרשרת (SCFAs), שהן קריטיות לבריאות במגוון מערכות הגוף. ניתן לשפר את ייצור ה-SCFAs התלוי במיקרוביוטה באופן יעיל על ידי אימוץ דיאטות עשירות בסיבים, כגון תזונה ים תיכונית, טבעונית או צמחונית. בנוסף, צריכת תכשירים פרהביוטיים כמו FOS, GOS ואינולין, וכן פרוביוטיקה המכילה זנים מסוימים (כדוגמת Lactobacillus plantarum, Lactobacillus paracasei וזני Lactobacillus אחרים), יכולה לתרום משמעותית לקידום בריאות המעי והפחתת דלקתיות.
בנוסף לגישות אלו, הסקירה מדגישה את הפוטנציאל המבטיח של הפוסט-ביוטיקה כגישה טיפולית חדשנית. היא מתארת את יכולתם של תכשירים פוסט-ביוטיים – המכילים מטבוליטים ותרכובות ביו-אקטיביות מחיידקים לא חיים (כדוגמת SCFAs, פפטידים ופוליסכרידים חוץ-תאיים – EPS, המופקים בעיקר מנגזרות של חיידקי Lactobacillus ו-Bifidobacterium) – לווסת תהליכים דלקתיים ולחזק את בריאות המעי. יתרונה הבולט של הפוסט-ביוטיקה טמון ביציבותה הגבוהה ובפרופיל בטיחות משופר בהשוואה לפרוביוטיקה חיה, מה שהופך אותה לאלטרנטיבה אטרקטיבית עבור אוכלוסיות רגישות. מוצרים אלו מציעים תמיכה במצבים כמו מחלות מעי דלקתיות (IBD), מחלות אוטואימוניות, תסמונת מטבולית, מחלות כבד וכליות, ומצבים הקשורים לדלקת כרונית ודיסביוזיס במעי.
למרות שאין המלצה למוצר פוסט-ביוטי ספציפי כיום, הבנת הפוטנציאל הגלום בהם, יחד עם גישות תזונתיות ופרו/פרה-ביוטיות, מאפשרת לכל אחד לבחון דרכים מגוונות לתמוך בבריאות המעי והגוף כולו. חשוב להמשיך לעקוב אחר ההתפתחויות המדעיות בתחום זה ולהתייעץ תמיד עם איש מקצוע בתחום הבריאות לפני נטילת תוספים.
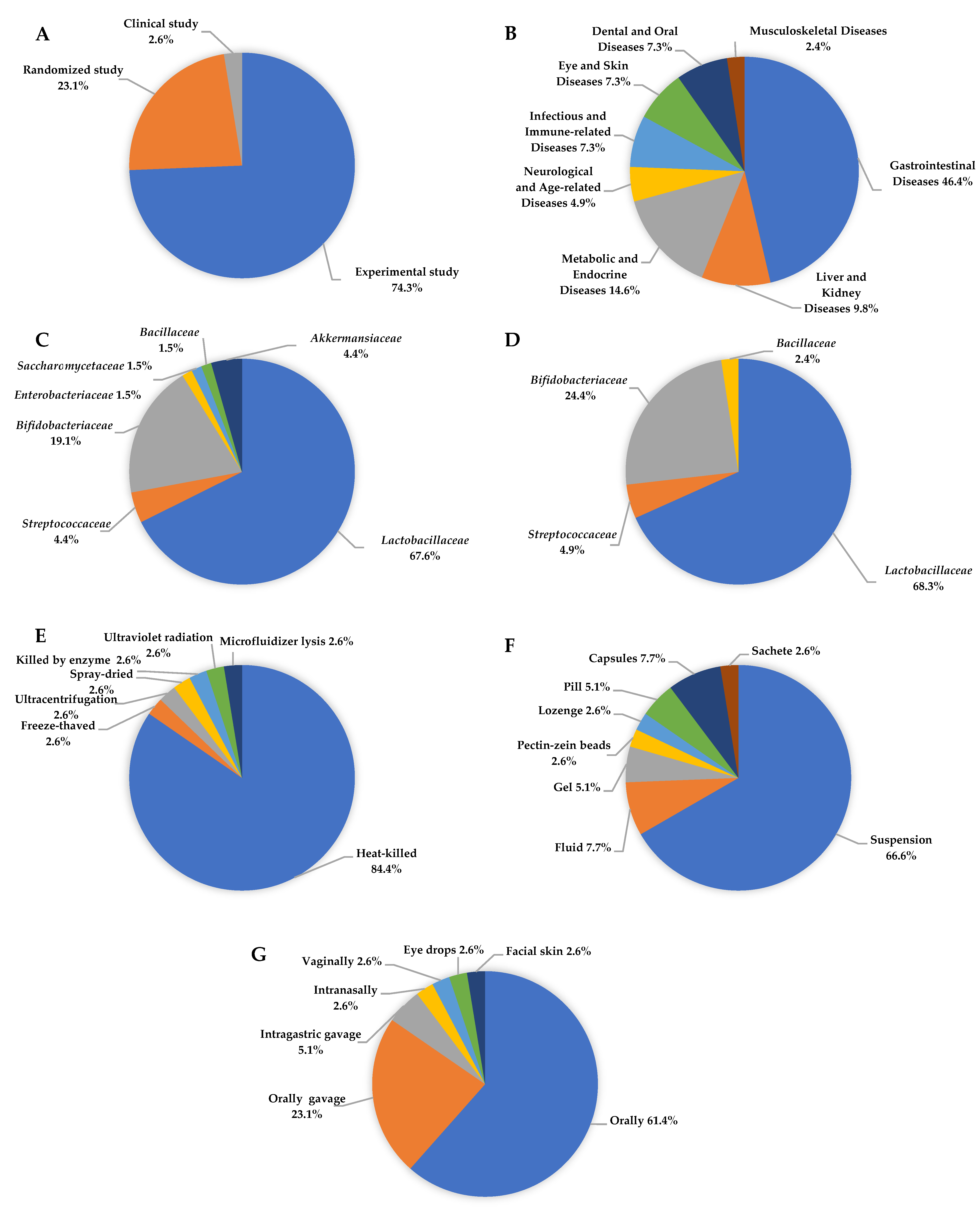
פרוביוטיקה חיה או מומתת ואם בכלל.
סיבים תזונתיים – מזון פרהביוטי – בריאות כללית.
היי לך.. אני משקיע שעות רבות כל יום באיתור ותרגום מאמרים כדי לספק לכולם את המידע העדכני ביותר, לבריאות טובה בדרך הטבע. וכדי שאוכל להמשיך לספק את המידע ולתחזק את האתר. כל תרומה, גדולה או קטנה תהיה לעזר רב. לתרומה נוחה ופשוטה דרך Pay Pal.
מוזמנים להזין דוא"ל למטה כדי להתעדכן ראשונים





כתיבת תגובה