לפעמים כדי להסביר על רכיב מסוים צריך להכנס קצת יותר לעומקם של דברים. הטבע הוא דבר מורכב וכל מרכיב כימי יכול להיות חשוב ביותר במידה מסוימת של צריכה ומזיק לאנשים מסויימים במידה גבוהה יותר של צריכה. ואיזון הוא הקו המנחה.
לכל אדם יש DNA ייחודי לו, שמועבר דרך העץ המשפחתי לדורותיו. DNA היא חומצת גרעין שבנויה משרשרת של נוקליאוטידים (גדיל), וההבדל בין בעלי חיים ובני אדם הוא השוני בהרכב שרשראות הנוקליאוטידים.
הנוקליאוטידים שבונים את סלילי ה- DNA הם אדנין, גואנין, תימין וציטוזין (A,G,T,C בהתאמה). ב-RNA לא מופיע תימין, ובמקומו מופיע אורציל (U).
*** הערת שוליים: ה-RNA היא מולקולה נוספת של נוקלאוטידים שמקורה ב- DNA והיא אחראית בעיקר על יצירת חלבונים בתוך התא על ידי הריבוזום.
הגוף זקוק למיליארדי נוקלאוטידים כדי ליצור עותקים חדשים של DNA בכל פעם שתא מתחלק. הוא יכול להשיג אותם על ידי הצלתם מחלבונים ישנים, סינתזה מחומצות אמינו כגון גלוטמין וסינתזה מסוכרים. וכמובן דרך התזונה (אגוזים, שקדים, גרעינים ויתר זרעי מאכל, פירות, ירקות ופטריות).
אחד התפקידים העיקריים של נוקלאוטידים הוא ריפוי ותיקון המעיים[1][2][3], במיוחד באזורים של חולשת מעיים. יש לכך חשיבות מיוחדת עבור אלו המתמודדים עם מצבים הקשורים למעיים כגון תסמונת המעי הרגיז (IBS), קוליטיס כיבית ומחלת קרוהן[4], אך גם עבור מצבים אוטואימוניים, סוכרת וסרטן.
מחקר שפורסם בכתב העת Gut העלה כמה תגליות מרגשות לגבי התפקוד והחשיבות של נוקלאוטידים במערכת העיכול. נמצא שמערכת העיכול דורשת אספקה מתמשכת וכבדה של נוקלאוטידים המיוצרים על ידי הכבד. עוד נמצא במחקר שכאשר מיוצרים מספיק נוקלאוטידים לצרכי מערכת העיכול, ניתן לראות מספר יתרונות, כולל שיפור בצמיחה מחודשת של הכבד והגברת היענות המערכת החיסונית – במיוחד נגד חיידקים אופורטוניסטים. הם גם מזהירים שהרגלי אכילה רעים עלולים להפחית מהגוף את האנרגיה לייצור נוקלאוטידים באופן פנימי.
נוקלאוטידים נמצאו גם כמשפרים את מצבם של כיבים במעי הדק[5], מעודדים תיקון מעיים לאחר אכילת מזונות בעייתיים כמו אכילת גלוטן, שתיית אלכוהול או שימוש בתרופות למשל NSAIDs, ועשויים לסייע ב"הגנה על רירית המעי" – שהיא מנגנון של מערכת החיסון.
חוסר בנוקלאוטידים תזונתיים עשוי לשחק תפקיד בשלבים המוקדמים של הסרטן[6]. מחקר משותף של חוקרים מהאוניברסיטה העברית בירושלים והמרכז הרפואי של אוניברסיטת מישיגן מצא שאונקוגנזה עשויה לנבוע מרמות נוקלאוטידים לא נאותות שאינן יכולות לתמוך בשכפול DNA וביציבות התקינה של גנים[7].
ומדוע כל ההסבר הזה?
כי היום אני מעוניין להעביר לכם מידע חשוב על תרכובות שנקראות פורינים, מהן נגזרות שתי מולקולות של נוקליאוטידים החשובים בייצור DNA ו-RNA. והן גואנין ואדונין. וזה ללא צל של ספק חשוב ביותר לבריאות שלנו.
הפורינים נמצאים בהמון רכיבי מזון (פירוט מקיף בתמונה למטה) ויש אותו גם במשקאות אהובים כמו קקאו, קפה ותה (קפאין ותיאוברומין).
המזונות מחולקים ל- 5 רמות של מינונים של פורינים:
נמוכה מאוד – פחות מ-50 מ"ג ל-100 גרם מזון
נמוכה – בין 50-100 מ"ג
בינונית – 100-200 מ"ג
גבוהה – 200-300 מ"ג
גבוהה מאוד – 300 מ"ג ומעלה
אם תכנסו לרשימה המצולמת, אתם תבינו שהחומר הזה קיים כמעט בכל מזון באיזו שהיא רמה. כאשר הבולטים ברמות הגבוהות הם בשר ופירות ים.

אכילת מזונות המכילים פורינים גורמת לרמות גבוהות יותר של חומצות שתן. אצל אנשים בריאים שאוכלים מזונות המכילים פורינים כ-30% נשפכים כבר במעי[8] דרך הצואה ורוב חומצות השתן שנכנסות למחזור הדם מנוקות על ידי הכליות.
היפראוריקמיה (HUA) היא הפרעה מטבולית המתבטאת בהפרעות בחילוף החומרים של פורינים, מה שמוביל לעלייה בריכוז חומצת השתן (UA) בסרום. שכיחות HUA ברחבי העולם נמצאת במגמת עלייה, בעיקר בהשפעת שינויים באורח החיים ובהרגלי התזונה.
היפראוריקמיה הוא הגורם העיקרי התורם לגאוט – מצב דלקתי המשפיע על המפרקים. זה נפוץ יותר אצל גברים מאשר אצל נשים. והמצב כמובן מלווה בכאב מפרקים עד השבתה של פעילות.
בין השנים 1990-2021, שכיחות גאוט העולמית עלתה ב-10%[9]. בסך הכל 7.44 מיליון מקרים של גאוט נאמדו ברחבי העולם בשנת 2017[10]. מדובר בעלייה ניכרת במהלך 25 השנים האחרונות והתחזיות מצביעות על כך שתמותה מגאוט עשויה לעלות ב-55% ב-2060.
היפראוריקמיה אינה רק הגורם העיקרי התורם לגאוט, אלא גם קשורה למחלת כליות כרונית (CKD), אירועים קרדיווסקולריים ותסמונת מטבולית, דבר המדגיש את חשיבותה כבעיה בבריאות הציבור בקנה מידה עולמי.
עכשיו.. אם נחזור רגע לתמונה שלמעלה. ניתן לראות שבמרבית הפירות והירקות המינון הוא נמוך עד נמוך מאוד וזו למעשה סיבה נוספת שהתזונה שלנו צריכה להיות מבוססת פירות וירקות, גם במרכיב הזה החשוב ל-DNA של התא וגם כי זו התזונה המיטיבה ביותר עם מיגוון המיקרוביום. על אחת כמה וכמה כאשר יש כבר תסמינים של עודף. כמו אבני חומצה אורית (בכליות) או במפרקים (גאוט). אנשים עם נטיה לתופעות אלה או כשהם כבר במצבים הללו כדאי שיעברו על התמונה כדי לדעת אילו מזונות עדיפים להם ואילו מומלץ להגביל עד להמנע.
וכדי להוסיף עוד עדויות.. סקירות ומטה אנליזות שמראות שתזונה מבוססת מהחי מעלה את הרמות של חומצה אורית[11][12][13] הרבה יותר ממקורות צמחיים, שנמצאו גם עם שכיחות נמוכה יותר של גאוט[14][15][16][17].
ראיות מצטברות מצביעות על כך שדפוסי תזונה ארוכי טווח ממלאים תפקיד קריטי בעיצוב המבנה והתפקוד של המיקרוביום ותזונה עשירה בסיבים תזונתיים, פוליפנולים ושומנים בלתי רוויים קשורה למגוון מיקרוביאלי גדול יותר ולשפע מוגבר של טקסונים מועילים, בעוד שתזונה עתירת שומן, סוכר גבוה ותזונה מעובדת במיוחד קשורה לדיסביוזה ולהפרעות מטבוליות[18][19].
הקשר למיקרוביום
מחקר שפורסם ביוני 23 בג'ורנל Cell Host & Microbe בהובלת חוקרים מאוניברסיטת Wisconsin–Madison ושותפים נוספים מרחבי העולם זיהו חיידקים המסוגלים לפרק חומצת שתן בסביבה דלת החמצן של המעיים ואת הגנים הספציפיים המאפשרים את התהליך. הם מתארים דרך חדשה שבה חיידקי מעיים עשויים להשפיע על בריאותנו ודרך פוטנציאלית לטיפול בגאוט או במניעת מחלות לב.
המעבדה של Federico E. Rey שיתפה פעולה עם חוקרים בשוודיה שניתחו גורמים הכוללים רובד עורקי, רמות חומצת שתן וקהילות מיקרוביאליות במערכת העיכול בקבוצה של כמעט 1,000 אנשים.
המחברים מציינים שכמות חומצת השתן בגופם הלכה יד ביד עם כמות השומנים, הכולסטרול ודברים אחרים המסיידים את העורקים שלהם.
הרמות של חומצת השתן התאימו גם לדפוסים של חיידקים שונים הנמצאים במעיים של אנשים אלה. לכן, הם רצו לדעת אם יוכלו לזהות את סוגי החיידקים הקשורים לחומצת שתן נמוכה יותר ולראות אם הם קשורים לטרשת עורקים נמוכה יותר.
לכן הם ביצעו השתלות צואה כדי להעביר חיידקי מעיים מעכברים בוגרים לעכברים שנולדו ללא חיידקים. בריאות העורקים עברה יחד עם החיידקים המושתלים – עכברים שקיבלו חיידקים מתורמים עם עורקים כבדי פלאק ורמות גבוהות יותר של חומצת שתן בדמם פיתחו את אותם מצבים. עכברים שקיבלו חיידקים מתורמים עם פחות חומצת שתן וכלי דם צלולים יותר היו נמוכים יותר בשני המדדים.
החוקרים החלו לזהות את החיידקים הקשורים לתוצאות בריאות, תוך ניטור הגנים שהיו פעילים במיוחד כאשר החיידקים גדלו על חומצת שתן. הממצא הזה הוביל את החוקרים למקבץ של גנים, שנמצאו על פני סוגים רבים ושונים של חיידקים, הנחוצים לפירוק פורינים וחומצת שתן במעי. החוקרים מסבירים שכאשר החיידקים המפרקים את הפורינים השתמשו בחומצת שתן במעיים לצרכיהם, הייתה פחות חומצת שתן בדם של העכברים.

בשלב הבא החוקרים יבחנו האם השתלת חיידקים אוכלי פורינים אצל עכברים עם בעיות רובד עורקים, יכולה לתקן את מחלת הלב וכלי הדם שלהם.
ועד אז…
איך שומרים על מיקרוביום מגוון ובריא?
תזונה מגוונת מבוססת צומח[1] (כל הצבעים, כל הטעמים, כל המרקמים), כל המשפחות (פירות וירקות עם קליפה, דגנים מלאים, קטניות, אגוזים, שקדים, זרעים ונבטים ומונבטים) וגם בתוך המשפחות לגוון לדוגמה: ירוקים זה לא רק חסה ופטרוזיליה. זה גם מנגולד, רוקט, רוקולה, תרד, סלרי, בזיליקום, נענע ועוד ועוד. עדשים זה גם ירוק, צהוב, כתום, חום, שחור, קטניות יש עשרות סוגים. כאשר יש סייג אחד. מה שלא עושה טוב. מורידים!
דרכים נוספות לקבל לחיזוק החיידקים הטובים: סיבים תזונתיים, עמילנים עמידים ומזון מותסס: כרוב כבוש (sauerkraut)[1], קימצ'י (קוראני), טמפה (אינדונזי), נאטו ומיסו (יפני), משקה קומבוצ'ה. וכמובן התססת פירות וירקות ביתית. והמדריך הבא לדעתי הוא השלם ביותר חלק 1, חלק 2. ישנה גם הדרכה דרך סרטונים אחרי הרשמה כאן.
במקביל להמנע ממגע וצריכה של:
תרופות המשנות לרעה את הרכב המיקרוביום במיוחד אנטיביוטיקה, אבל גם נוגדות חומציות (PPI), מטפורמין, לקסטיבים, תרופות נוגדות דיכאון (SSRI), סטרואידים ונוגדי דלקת שאינם סטרואידים.
חומרי חיטוי (אנטיבקטריאליים) המכילים למשל טריקלוזן.
תכשירים המכילים משבשי אותות אנדוקריניים כגון פתלאטים ו'חומרים אורגניים מופלרים, PFAS, BPA, מעכבי בעירה, מזונות מרוססים[2][3] ואולי במיוחד גלייפוסט. וגם פלסטיק.
מזון מעובד[2][3][4][5]/ ומזון מסוכר.
*** תוספת מאי 25
מחקר שפורסם במאי 25 בכתב העת Frontiers in Nutrition בחן את הקשר בין מדד התזונה למיקרוביום המעי (DI-GM) לבין היפראוריקמיה באמצעות נתונים מסקר הבריאות והתזונה הלאומי NHANES – מחקר חתך המשתמש בשיטת דגימה הסתברותית רב-שלבית כדי להעריך את המצב התזונתי והבריאותי.
החוקרים מציינים שמחקרים מצביעים על כך ששינויים במיקרוביום המעי עשויים להשפיע על חילוף החומרים של חומצה אורית דרך מסלולים הכוללים פירוק פורינים, ייצור מטבוליטים מיקרוביאליים והפרשת חומצה אורית החוצה. הם מוסיפים שמדד DI-GM הראה קשרים עקביים הפוכים עם מספר מצבים כרוניים מטבוליים ולכן במחקר הנוכחי הם בחנו את הקשר להיפר אוריקמיה.
DI-GM הוא מדד חדש המשקף את מגוון מיקרוביום המעי בהקשר של מזונות. כלומר מבטא את הקשר בין מזונות או קבוצות מזון לאופי מיקרוביום המעי.
מדד זה מסוכם במונחים של ראיות להשפעה מועילה, שלילית או ללא השפעה נצפית, על מדדי גיוון חיידקי ( α ו-β), רמות חומצות שומן קצרות שרשרת (בוטיראט, אצטט, פרופיונאט, איזובוטיראט – SCFA) בצואה ושינוי ביחסי המערכות וחיידקים ספציפיים.
כאשר רכיבים מיטיבים כוללים: חומוס, סויה, דגנים מלאים, סיבים תזונתיים, חמוציות, אבוקדו, ברוקולי, מוצרי חלב מותססים, קפה ותה ירוק.
רכיבים שליליים כוללים: דגנים מזוקקים, בשר אדום, בשר מעובד ויותר מ-40% מהאנרגיה היומית משומן רווי וטרנס.
השפעה מיטיבה הוגדרה כעלייה ב:
Faecalibacterium, Bifidobacterium, Lactobacillus, Lactococcus, Parabacteroides, Roseburia,
Eubacterium rectale, Eubacterium hallii, Akkermansia, Prevotella, Prevotella copri, Anaerostipes, Anaerostipes hadrus, Veillonellaceae, Parabacteroides distasonis, Gemmiger, ו- Moraxellaceae .
וירידה ב:
Bacteroides, Bacteroides fragilis, Fusobacteria, Streptococcus, Clostridium, Clostridium symbiosum, Clostridium perfringens, Dialister, Alistipes, Bilophila, Ruminococcus gnavus, Dorea, Actinomyces, Odoribacter, Blautia, Lachnospira, Lachnospiraceae, Sutterella, Enterobacteriaceae, ו- Klebsiella sp.
המדד כולל בתוכו שיטת ניקוד כאשר על כל מזון חיובי שנצרך מעל החציון של משתתפי המחקר מקבלים נקודה. ולהיפך, על כל מזון שלילי שנצרך מתחת לחציון של משתתפי המחקר מקבלים נקודה.
הציונים הללו מחולקים בדרך כלל לקבוצות (לדוגמה: 0-3 נקודות, 4 נקודות, 5 נקודות, ו-6 נקודות ומעלה).
נבדקי המחקר היו מבוגרים בגיל 18 ומעלה שהשלימו סקרים תזונתיים ומבחני חומצה אורית. קריטריוני ההדרה היו אנשים עם נתונים חסרים או לא שלמים. סך הכל 25,899 אנשים עמדו בקריטריונים.
היפר אוריקמיה הוגדרה אצל גברים כגבוה מ-7 מ"ג/ד"ל בצום ואצל נשים גבוה מ-6 מ"ג/ד"ל.
החוקרים גם התייחסו לגורמים מבלבלים: גיל מצב סוציואקונומי (PIR), עישון, צריכת אלכוהול, מדד BMI; ומחלות רקע, כולל יתר לחץ דם, סוכרת, היפרליפידמיה ומחלת כליות כרונית.
המשתתפים סווגו לארבעה רבעונים נפרדים לפי ציוני DI-GM שלהם: רבעון 1 ציון 0-3, רבעות 2 ציון 4, רבעון 3 ציון 5 ורבעון 4 ציון 6 ומעלה.
ניתוח רגרסיה לוגיסטית שימש להערכת הקשר בין DI-GM להיפראוריקמיה.
שלושה מודלים עברו הערכה: מודל 1 (ללא התאמה למבלבלים); מודל 2 (התאמות לגיל, מין, גזע, רמת השכלה, מצב משפחתי ומצב סוציואקונומי; ומודל 3 (התאמות לעישון, צריכת אלכוהול, מדד מסת גוף, יתר לחץ דם, סוכרת, היפרליפידמיה ומחלת כליות כרונית).
הניתוח גילה קשר הפוך מובהק בין ציוני DI-GM גבוהים יותר לבין הסבירות להיפראוריקמיה.
- במודל 1 כל עלייה של יחידה בציון DI-GM תאמה לירידה של 3.9% בסיכון להיפראוריקמיה.
- במודל 2 כל עלייה של יחידה בציון DI-GM תאמה לירידה של 4.6% בסיכון להיפראוריקמיה.
- במודל 3 כל עלייה של יחידה בציון DI-GM תאמה לירידה של 3.2% בסיכון להיפראוריקמיה.
- בהשוואה בין רבעונים הסיכון להיפראוריקמיה היה נמוך יותר (10.3%-) ברבעון הגבוה לעומת הנמוך.
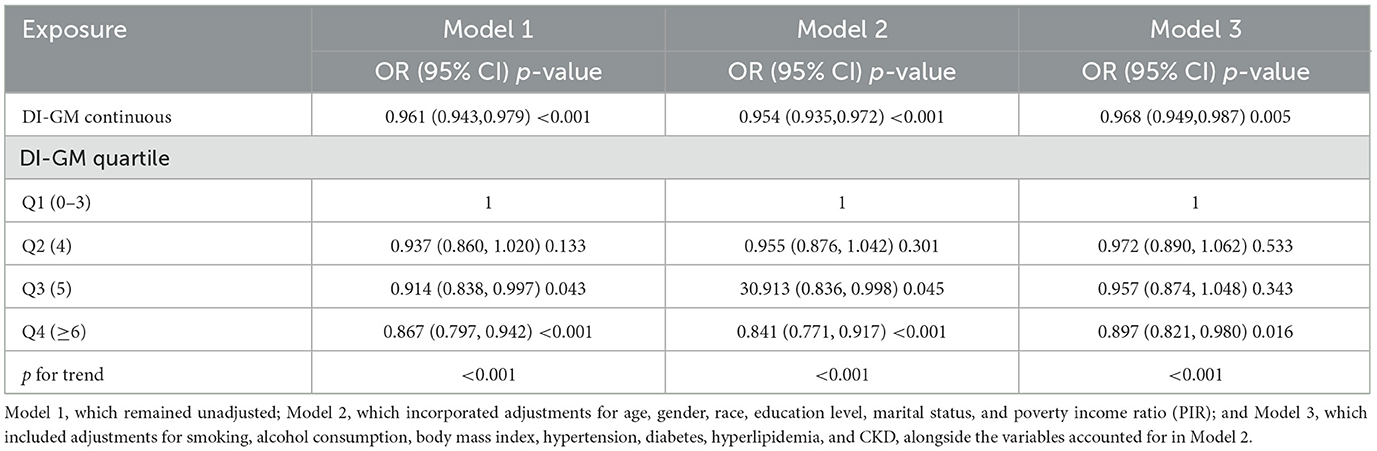
- ניתוח הרגרסיה המחיש עוד יותר קשר שלילי ליניארי בין ציוני DI-GM לבין הסיכון ל-HUA.
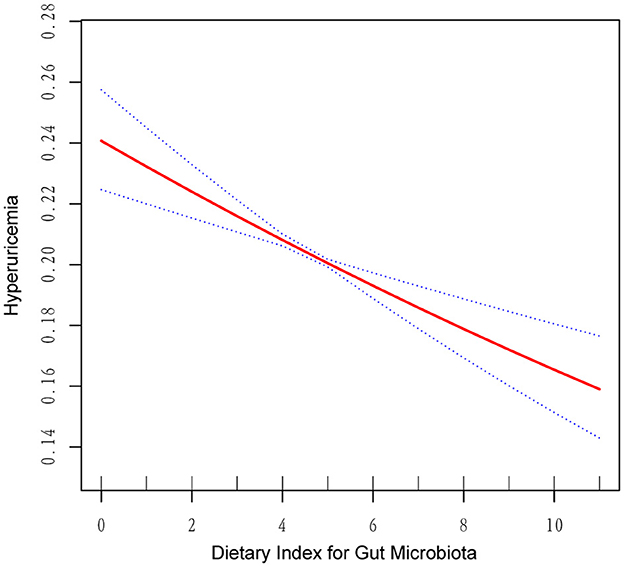
- מספר רכיבים שסווגו כמועילים למיקרוביוטה של המעיים הראו קשרים הפוכים מובהקים סטטיסטית עם היפראוריקמיה.
- צריכה גבוהה יותר של סיבים תזונתיים (24.9%-).
- דגנים מלאים (17.3%-).
- מוצרי חלב מותססים (10%-).
- אבוקדו (21.4%-).
- חמוציות (16.2%-).
- חומוס (38.9%-).
- קפה (8%-).
החוקרים מציגים חלק מהמנגנונים האפשריים:
- סיבים תזונתיים מעודדים את צמיחתם של חיידקים מועילים, אשר בתורם מפחיתים את סינתזת החומצה האורית על ידי עיכוב אנזימים מרכזיים כמו קסנטין אוקסידאז בכבד. בנוסף, סיבים תזונתיים משפרים את תנועתיות המעי, ומפחיתים את ספיגת הפורינים.
- חומצות שומן קצרות שרשרת (SCFAs) הן המטבוליטים העיקריים הנוצרים באמצעות תסיסה של סיבים תזונתיים על ידי חיידקי המעי. חומצות שומן קצרות שרשרת משמשות כמקור אנרגיה לתאי האפיתל של המעי, ומסייעות בהפרשת חומצה אורית.
- פוליפנולים מעכבים את האנזים קסנטין אוקסידאז ומווסתים טרנספורטרים של חומצה אורית. פוליפנולים גם הוכיחו את היכולת להגביר את אוכלוסיית החיידקים המועילים, כולל Bifidobacterium, Lactobacillus, Bacteroides ו-Prevotella. במקביל, הם מפחיתים את השפע היחסי של Proteobacteria ומשנים את יחס Firmicutes-to-Bacteroides, ובכך פועלים כפרה-ביוטיקה.
ומהכיוון ההפוך
- מחקר שהציג שתזונה עתירה בשומן מעלה חומצה אורית. וחיידק L.plantarum הדגים את היכולת למתן את העלייה .
- מחקר תצפיתי מוצלב בן 10 שבועות, 20 מבוגרים בריאים השתתפו בצריכת שתי דיאטות איזוקלוריות: אחת עשירה בדגנים מלאים ובסיבים, והשנייה מורכבת בעיקר מבשר אדום. צריכת בשר אדום גרמה לשינויים ניכרים במיקרוביום המעי, במיוחד בכל הנוגע לשכיחות Firmicutes, והייתה קשורה לרמות גבוהות של חומצה אורית וקריאטינין.
החוקרים מסכמים שמחקר זה בוחן ביסודיות את יחסי הגומלין בין DI-GM לבין התרחשות היפראוריקמיה, ומספק תובנות חדשות לגבי הקשרים המורכבים בין תזונה, קהילות מיקרוביאליות ומטבוליזם של חומצה אורית. הם קוראים גם לעשות מחקרים נוספים כדי למצוא את הקשר הסיבתי בין תזונה-מיקרוביום-מחלות.
הקשר לפחמימות
- *** תוספת מאי 24
מחקר שפורסם במאי 24 בכתב העת JAMA בוחן את היתרונות הפוטנציאליים של תזונה מבוססת צומח על סיכון גאוט.
המחקר השתמש בנתונים של אמריקאים שנרשמו ל-Health Professional Follow-Up Study, שנערך בין השנים 1986-2012, ובמחקרי האחיות שנערכו בין השנים 1984-2010. כל משתתפי המחקר היו נקיים מגאוט בתחילת המחקר.
מטרת המחקר הייתה למדוד חשיפה ממוצעת לאינדקס תזונה מבוסס צומח בריא (hPDI) ולא בריא (uPDI). מדדים אלו חושבו על סמך 18 קבוצות מזון שנקבעו באמצעות שאלון תדירות מזון.
המחקר כלל כמעט 123,000 משתתפים, עם גיל ממוצע של 54 ו-50.9 עבור גברים ונשים, בהתאמה. במהלך תקופה של כמעט 2.8 מיליון שנות אדם, דווח על הארעות חדשה של גאוט ב-2,700 אנשים.
התוצאות מצאו ש- hPDI היה קשור באופן הפוך ומובהק (21%-) לסיכון לגאוט, בעוד שה-uPDI היה קשור באופן חיובי לסיכון לגאוט (17%+), במיוחד בנשים (31%+).
מזונות בריאים ללא סיכון נלווה למחלת גאוט כללו פירות, ירקות, אגוזים וקטניות. - *** תוספת ספטמבר 24
מחקר שפורסם באוגוסט 24 בכתב העת Nutrients בחן את ההשפעות של כמות, סוג ומקור פחמימות (סיבים, עמילנים ממקורות שונים, סוכרים מהמזון וסוכרים מוספים כחומר גלם) בשילוב עם נטיה גנטית אינדיבידואלית על הסיכון להתפתחות גאוט. הם גם חקרו סמנים ביולוגיים של שתן וסרום שמתווכים את הקשר בין צריכת פחמימות לבין הסיכון למחלת גאוט.
המחקר כלל 187,387 משתתפים מהביובנק הבריטי בגילאי 40-69.
החוקרים הגבילו את הניתוח לאנשים שצורכים דיאטות קבועות.
המחקר מצא שהצריכה הכוללת של פחמימות הייתה קשורה לירידה של 28-33% בסיכון לגאוט כלומר יש קשר הפוך בין פחמימות לגאוט. הממצאים הללו בלטו עוד יותר אצל האנשים עם נטייה גנטית לגאוט. הפחמימה היחידה שנמצאה מעלה סיכון (15%) היא הסוכר המוסף/המעובד.

מזונות ורכיבים שיודעים להוריד רמות של חומצה אורית:
- מזונות מהצומח
- צמחי מרפא/ חליטות
- מורינגה.
- קינמון [1] יחד עם חרצית [2][3][4] מונעים מאנזים xanthine oxidase לייצר חומצה אורית.
- כורכום (כורכומין) מונע מאנזים xanthine oxidase לייצר חומצה אורית [1][2].
- ג'ינג'ר [1].
- קצח (טימוקווינון) [1].
- תה ירוק (פוליפנולים ו- EGCG) [1][2][3].
- צמח הקערורית (סקוטלריה), שמכיל חומר פעיל בשם Baicalein [1]
- עלי זית [1].
- לחך [1].
- רוז היפ [1].
- עלי גויאבה [1].
- אשווגנדה [1][2].
- משקאות
- נוגדי חמצון/ תוספים
- ויטמינים ומינרלים
- פרוביוטיקה [1][2][3][4][5][6][7]. והחיידקים שנמצאו מועילים: Bifidobacterium longum, L. fermentum, L. plantarum, L. rhamnosus, L. fermentum, L. gasseri
- טיפוס מדרגות [1].
גורמים נוספים לגאוט מהם מומלץ להמנע גם כן (דומה מאוד לאבנים בכליות)
- סוכר (פרוקטוז) [1][2][3][4][5].
- אלכוהול במיוחד בירה ומשקאות חריפים, בשר, פירות ים, משקאות קלים ממותקים וצריכת מזונות עתירי פרוקטוז [1].
- מזונות מעובדים [1].
יש עוד סוגים של אבנים בכליות על רקע חומצה אוקסלית. עליהם תוכלו לקרוא במאמר: "אבנים בכליות – קצח מול פלסבו ודברים נוספים למניעה וטיפול"
מאמר מקיף נוסף על מניעה וניהול אבנים בכליות על ידי צמחים [1].
היי לך.. אני משקיע שעות רבות כל יום באיתור ותרגום מאמרים כדי לספק לכולם את המידע העדכני ביותר, לבריאות טובה בדרך הטבע. וכדי שאוכל להמשיך לספק את המידע ולתחזק את האתר. כל תרומה, גדולה או קטנה תהיה לעזר רב. לתרומה נוחה ופשוטה דרך Pay Pal.
מוזמנים להזין דוא"ל למטה כדי להתעדכן ראשונים





כתיבת תגובה