מחלת הפרקינסון תוארה לראשונה על ידי רופא וחוקר אנגלי בשם דר' ג'יימס פרקינסון בשנת 1817, כמחלה קשה המלווה ברעד, נוקשות שרירים, בעיות הליכה, גוף כפוף ונפילות. שכיחותה של מחלת הפרקינסון עולה עם הגיל, ולאחר גיל 65 היא מאובחנת אצל 1% מהאוכלוסיה. ההערכה היא כי בישראל חיים כ-25,000 חולים המתמודדים עם פרקינסון.
לפי קרן פרקינסון, יותר מ-60,000 אנשים מאובחנים עם פרקינסון מדי שנה בארצות הברית, ויותר מ-10 מיליון אנשים ברחבי העולם חיים עם המחלה[1].
מחלת פרקינסון היא מחלה נוירודגנרטיבית מתקדמת המאופיינת באובדן של נוירונים דופמינרגיים וקשורה להצטברות לא תקינה של החלבון α-synuclein במוח. יש הסוברים שגם הצטברות של חלבון TAU (שקשור על פי רוב בחולי דמנציה ואלצהיימר), מהווה גורם גם בפרקינסון ואולי אפילו השחקן הראשון שגורם לתסמינים המוטוריים הקרדינליים של המחלה[2].
דופמין הינו מוליך המשמש בין היתר להעברת מסרים עצביים בין גרעיני הבסיס (אזור במח שאחראי על איכות התנועה) לבין השרירים.
המחלה מאופיינת בשילוב של הפרעות מוטוריות: איטיות בתנועה, נוקשות שרירים, רעד במנוחה, הפרעה בשיווי משקל, הפרעות הליכה ונפילות, קיפאון בהליכה, שינויים בכתב יד ותנועות בלתי רצוניות.
והפרעות שאינן מוטוריות: הפרעות דיבור, הפרעות בליעה הפרעות במערכת העיכול, דיכאון, אובדן מוטיבציה, ירידה קוגניטיבית, הפרעות בזיכרון, נפילות לחץ דם, הפרעות במתן שתן, הפרעות בתפקוד המיני, הזעת יתר, סבוראה בעור ועוד.
גורמים ומנגנונים אפשריים
על פי הרפואה המחלה נגרמת משילוב של גנטיקה (10%) ומזהמים סביבתיים (90%). כלומר מדובר בחשיפה כרונית לכימיקלים מייצרי עקה חמצונית ואולי במיוחד לחומרי הדברה (גלייפוסט, פירתרואידים, אורגנופוספאטים [2], פאראקווט, רוטנון [1][2][3]), לזיהום אוויר [2][3], ננו-פלסטיק, טריכלורואתילן וכל שאר הדברים שמשנים לרעה את הרכב המיקרוביום כמו אנטיביוטיקה, נוגדי דלקת שאינם סטרואידם (NSAIDS),שכן הם חלק חשוב ועיקרי בייצור דופמין. כל אלה כמובן בשם ה"קידמה", הנוחיות וה"דאגה לציבור" .
*** במפגש השנתי של החברה למדעי המוח Neuroscience 2022 חוקרים הציגו 3 ממצאים שמאששים את האמור למעלה:
- מצוקות בחיים המוקדמים קשורות לחוסר איזון מיקרוביאלי במעיים, רמות גבוהות יותר של דלקת והבדלים במבנה המוח הקשורים למשקל.
https://www.abstractsonline.com/pp8/#!/10619/presentation/77588 - חשיפה לחומרי הדברה (פירתרואידים) דרך הפה יכולה לשנות את מסלולי הדופמין במוח ולהוביל לשינויים במיקרוביום המעי הרלוונטיים למחלת פרקינסון.
הקשרים המתעוררים בין מחלת פרקינסון, חשיפה לחומרי הדברה וחריגות במערכת העיכול הובילו לרעיון שחלק מהמקרים של המחלה עלולים להיגרם מתוך המעי לאחר חשיפה לחומרי הדברה דרך הפה.
עכברים טופלו דרך הפה בפירטארואיד (דלתאמטרין), דבר שהביא לשינוי התנהגויות מוטוריות ושינויים במסלולי הדופמין. בעכברים זכרים בלבד, חשיפה לדלתאמטרין עוררה גם התנהגויות מעיים המעידות על עצירות.
שינויים בהתנהגויות מוטוריות השתנו בשני המינים. כמו כן נצפה שחשיפה לדלתאמטרין שינתה משמעותית את רמות החלבונים החשובים לסינתזה של דופמין: Tyrosine hydroxylase (TH) ו- dopamine transporter (DAT)
https://www.abstractsonline.com/pp8/#!/10619/presentation/68083
החוקרים מסכמים שמחקר מדעי המוח ממחיש שכאשר מדובר בהפרעות מטבוליות ונוירולוגיות, איננו יכולים לכוון רק למוח, שכן לכל מה שקורה במעיים יש השפעה על המוח. הבנה טובה יותר של אינטראקציות בין המעי למוח תביא הזדמנויות נהדרות לאבחון, טיפול ומניעה של מחלות. - שינויים במיקרוביוטה של המעיים על ידי קוטל חרקים וקוטל עשבים (רוטנון), עשויים להוביל חלבונים מקופלים בצורה חריגה מהמעי הגס למוח, מה שמוביל לאובדן של נוירונים דופמינרגיים במחלת פרקינסון.
החוקרים פיתחו מודל עכבר של מחלת פרקינסון והזריקו למעיים שלהם רוטנון. הטיפול הוביל לליקויים מוטוריים המלווים באובדן של נוירונים דופמינרגיים במוח.
עכברים שטופלו ברוטנון הראו גם ביטוי מוגבר של α-synuclein במעי, במעי הגס ובמוח. הם גם חוו שינויים במיקרוביום במעיים שלהם שנמשכו עד 22 שבועות לאחר הטיפול.
התוצאות מצביעות על כך שמקורו של α-סינוקלאין לא תקין הינו מהמעי הגס ונודד למוח, מה שמוביל לאובדן נוירונים דופמינרגיים ולבעיות מוטוריות.
https://www.abstractsonline.com/pp8/#!/10619/presentation/68098
https://www.eurekalert.org/news-releases/968708
- *** תוספת אפריל 24
מאמר שפורסם באפריל 24 בכתב העת Journal of Parkinson's Disease מציע שהמחלה היא תוצאה של תהליכים שמתחילים במרכז הריח של המוח או במעיים, שכן הם מצופים ברקמה רכה חדירה, ולשניהם יש קשרים מבוססים היטב למוח. כלומר פרקינסון היא מחלה מערכתית, ששורשיה הראשוניים מתחילים באף ובמעיים וקשורים לגורמים סביבתיים כתורמים עיקריים, אם לא הגורמים, בה' הידיעה, למחלה.
הכימיקלים הללו גורמים להיווצרות אלפא-סינוקלאין רעיל.
החוקרים מסבירים שהכימיקלים הננשמים מגיעים ישירות למוח דרך עצב הנשימה והכימיקלים הנבלעים יכולים להשפיע דרך מערכת העצבים האנטרית (של מערכת העיכול) משם מתפשטת לשני צידי המוח וחוט השדרה.
החוקרים מציינים שלא כולם חווים פרקינסון – "התזמון, המינון ומשך החשיפה והאינטראקציות עם גורמים גנטיים[1] וסביבתיים אחרים הם כנראה המפתח לקביעה מי מפתח בסופו של דבר פרקינסון. ברוב המקרים, חשיפות אלו התרחשו ככל הנראה שנים או עשורים לפני התפתחות התסמינים".
המחברים מסיימים "בנוסף לפרקינסון, מודלים אלה של חשיפה סביבתית עשויים לקדם את ההבנה כיצד חומרים רעילים תורמים להפרעות מוחיות אחרות, כולל אוטיזם בילדים, ALS במבוגרים ואלצהיימר בקרב קשישים"
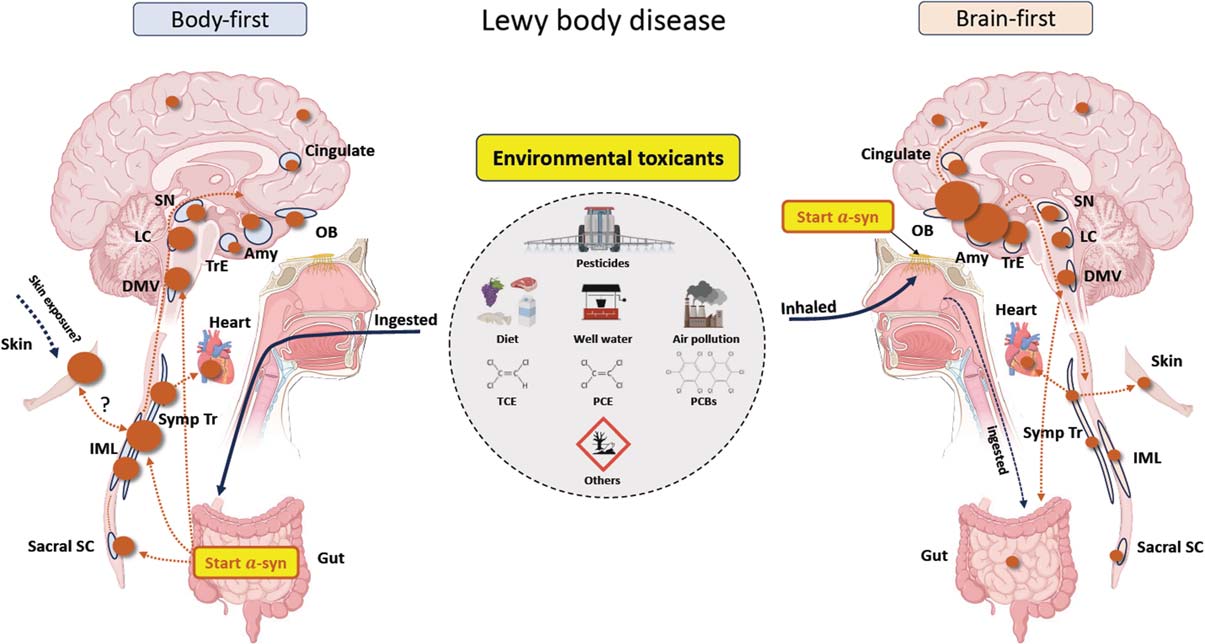
לכן בראש ובראשונה – להמנע ממזהמים סביבתיים לרבות אלה המשפיעים על המיקרוביום
החלק של המיקרוביום
אם יש משהו שדי משמח אותי מהצד המדעי של בריאות, הוא המחקר הרציני והמשאבים שמשקיעים בנושא המיקרוביום ושלמעשה מדובר בעולם ומלואו. עולם של מפעלים לייצור נוטריינטים. כאלה שמשפיעים על כל אספקט בריאותי ובסופו של דבר על כל איבר ועל כל מערכת.
מיקרוביום קיים בכל משטח בגוף שלנו, עור, ריאות, עיניים, לשון, כל איבר בעצם. אבל הכמות המירבית נמצאת במעיים, שם נעשית רוב הפעילות, והיא גם משפיעה על המיקרוביום והרכבו באיברים השונים.
החלק הפחות משמח הוא בפרקטיקה של הרופאים, שגם אם מבינים את המשמעות, אין להם כלים לחזק את המיקרוביום, למעשה יש להם רק כלים שפוגעים בו (תרופות).
המיקרוביום שלנו הוא למעשה הרפואה המונעת (בה' הידיעה) כי התפקיד שלו הוא הזנה ושיפור תפקודי מערכות ואיברים. ומחסור במיקרוביום או שינוי במיקרוביום יכול לייצר מגוון של בעיות מהקלות שבהן כמו גזים ונפיחויות ועד דלקות כרוניות, מחלות לב וכלי דם, השמנה, סוכרת, סרטן, בעיות רגשיות ובעיות עצביות כמו גם פרקינסון.
חשוב להבהיר שהרפואה מציגה את החיידקים כטובים ורעים. כאשר הרעים גורמים למחלות.
המדענים לעתים נותנים להם תכונות אנושיות כאילו הם עושים את זה בכוונת זדון ומטרגטים את החומר היישר למערכת זו או אחרת כדי ליצור שם פתולוגיה.
אז חיידקים אינם מחוללי מחלות, אין להם בקוד הגנטי להרוג או להחלות בני אדם. תפקידם הוא אקולוגי בלבד – פירוק רקמות וחומרים לרבות האוכל שנכנס לפה ממנו הם מייצרים גם מטבוליטים שונים בהתאם למה שמעיל בתוכו.
כלומר חיידקים הם חלק בלתי נפרד מאיתנו. הם היו כאן לפנינו ויישאר אחרינו. זה אנחנו שצריכים לשים לב למה שאנו אוכלים ושותים ונושמים ומורחים על העור. כי במידה ויהיה עודף חשיפה לחומרים תעשייתיים. יחולו שינויים בהרכב החיידקים ובמטבוליטים שהם מייצרים. לכן אם נאכל ג'אנק נקבל מטבוליטים רעילים ואם נאכל מזון מגוון בסיבים נקבל מטבוליטים מועילים.
כמו כן ייתכן מצב שבו אדם נחשף לכימיקלים לאורך שנים שפגעו ברקמה או איבר אז חיידקים יפרקו אותה ובמידה ואין את המרכיבים הנחוצים לשיקום והחלמה. זה מצב מסכן חיים. כמו במקרים של אלח דם בבתי חולים אצל מאושפזים שמגיעים עם מערכת חיסון לא מתפקדת ומחלות רקע כרוניות.
וזה חלק מהטבע. בדיוק כמו שתפוח שקיבל מכה – הוא יירקב כדי לחזור להזנת האדמה. זה לא החיידקים זו הפגיעה בפרי/איבר.
מאמרים המציגים את הקשר בין חיידקים לפרקינסון:
- במחקר שפורסם בג'ורנל הרפואי EBioMedicine ביוני 2019 בדקו את הרכב המיקרוביום אצל חולי פרקינסון במצב מתקדם של המחלה לעומת אנשים בריאים וראו הבדלים מהותיים במיקרוביום גם אחרי שנתיים של מעקב (עד כה נבדק ללא מעקב), כאשר אצל חולי הפרקינסון היה מחסור גדול בכמות ובזנים חשובים (Bifidobacterium, Prevotella, Lactobacillus, and Roseburia).
- מחקר מינואר 2020 בג'ורנל הרפואי Cell Reports במודל של תולעים, מראה מכניזם חדש של חיידק מועיל (פרוביוטיקה) בשם Bacillus subtilis שמאט ואפילו הופך מצב של הצטברות של רעילות שגורמת למוות של עצבים שאחראיים על ייצור דופמין וכשזה באזור המוטורי, מתחיל תהליך של פרקינסון.
- שני מאמרים שפורסמו בפברואר 22 בג'ורנל iScience ובמרץ 22 בג'ורנל scientific reports על ידי חוקרים ברזילאים מחזקים השערה זו ומתארים מנגנון שבאמצעותו התפתחות מחלת פרקינסון עשויה לנבוע בין השאר מדיסביוזיס.
המחקרים הראו שלעיתים קרובות פרקינסון מאובחן באיחור וכי מקורו עשוי להיות מוקדם הרבה יותר במערכת העצבים האנטרית [השולטת בתנועתיות מערכת העיכול], לפני שהוא מתקדם למוח דרך סיבים אוטונומיים.
פרסומים אחרונים דיווחו באופן עקבי על קיומו של דיסביוזיס במעיים בחולים עם פרקינסון ספורדי, מכיוון שהצורה הלא-תורשתית של המחלה ידועה, והראו כי החיידק Akkermansia muciniphila נמצא בשפע חריג בדגימות צואה של חולים אלה בהשוואה לקבוצת הביקורת.
החוקרים מציינים שתאים ספציפיים באפיתל המעי, הנקראים תאים אנטרואנדוקריניים, נמצאו לאחרונה כבעלי תכונות רבות דמויות נוירונים, כולל ביטוי של החלבון אלפא-סינוקלאין [αSyn]. ידוע כי פרקינסון ומחלות ניווניות אחרות קשורות להצטברות לא תקינה של חלבון זה. ומכיוון שהם נמצאים במגע ישיר עם לומן המעי – החלל שבתוך המעיים – ומחוברים באמצעות סינפסות לנוירונים האנטריים, תאים אנטרואנדוקריניים יוצרים מעגל עצבי בין דרכי העיכול ומערכת העצבים האנטרית. ככאלה, הם עשויים להיות גורם מפתח בהופעת פרקינסון במעיים.
מתוך ידיעה זו, קבוצת החוקרים יצאה לבדוק אם חומרים המופרשים על ידי חיידקים בשם A. muciniphila עשויים לעורר אגרגציה של α-Syn בתאים אנטרואנדוקריניים והאם ה-αSyn שמצטבר בתאים אלו יכול לנדוד לאחר מכן אל מסופי העצבים ההיקפיים במערכת העצבים האנטרית.
החוקרים עיבדו חלבונים המופרשים על ידי חיידקים אלה בהיעדר ריר מעיים ומצאו שהם מובילים לעומס יתר של סידן תוך תאי בתאים אנטרואנדוקריניים, ויוצרים עקה חמצונית על המיטוכונדריה שלהם, מעוררים סינתזה ושחרור מיני חמצן תגובתיים [ROS] שפוגעים במבנים תוך-תאיים וגורמים להצטברות של αSyn. וכאשר עיבדו יחד תאים אנטרואנדוקריניים ונוירונים, הם מצאו שניתן להעביר αSyn מצטבר מאחד לשני.
בצורה זו החוקרים הציגו שדיסביוזיס יכול להגביר את הצמיחה של חיידקים שיכולים לתרום להצטברות αSyn במעיים, ושהחלבון עשוי לנדוד למערכת העצבים המרכזית, ולהגדיר מנגנון אפשרי להתפתחות פרקינסון ספורדי.
החוקרים מציינים שמפל התגובות יכול להתחיל במעיים ולעלות אל המוח. ידוע שאנשים עם נטייה לפרקינסון ספורדית סובלים בדרך כלל מעצירות חוזרת שנים רבות לפני שהמחלה מתבטאת ובמחקר זה נמצא מתאם ישיר בין דיסביוזיס במעיים לפרקינסון.
החוקרים מסכמים שמחלות נוירודגנרטיביות הן חשוכות מרפא כרגע, לכן מניעתן צריכה להיות בבסיס העבודה. המחקר עד כה התמקד במוח, והתקדמות מועטה הושגה בכיוון זה במשך עשרות שנים. ולכן הם במקום זאת מתמקדים במעי. התגליות האחרונות נראות מבטיחות ביותר. הרבה יותר קל לווסת את המיקרוביוטה של המעי מאשר להתמודד עם הפרעה מבוססת במערכת העצבים המרכזית.
https://agencia.fapesp.br/research-reveals-how-gut-microbiota-imbalance-can-lead-to-parkinsons-disease/38424/ - מחקר של אוניברסיטת Alabama שפורסם בנובמבר 22 בג'ורנל Nature Communications, הראה חוסר איזון רחב בהרכב המיקרוביום אצל אנשים עם מחלת פרקינסון. לטענת החוקרים מדובר במחקר המיקרוביום הגדול ביותר שנערך ברזולוציה הגבוהה ביותר.
החוקרים השתמשו במטא-גנומיקה ממיקרוביום הצואה של אנשים עם PD ונבדקי ביקורת בריאים מבחינה נוירולוגית במטרה ליצור תצוגה מלאה, ללא שינוי של חוסר האיזון במיקרוביום של PD במעיים.
המחקר אכן מעיד על מיקרוביום מקדם מחלה.
החוקרים מצאו שפע יתר של פתוגנים אופורטוניסטיים ורכיבים אימונוגניים, המצביעים על זיהום ודלקת, ייצור יתר של מולקולות רעילות ושפע של תוצר החיידק curli. כל אלה יחד משרים את הפתולוגיה של PD וחוסר ויסות של נוירוטרנסמיטורים, כולל L-dopa. במקביל, היה מחסור במולקולות נוירו-פרוטקטיביות וברכיבים אנטי דלקתיים, מה שמקשה על ההחלמה.
צוות החוקרים רשמו 490 אנשים עם מחלת פרקינסון ו-234 אנשים בריאים. קצת יותר ממחצית מהנבדקים היו גברים והיו בעיקר מבוגרים מגיל 50. כולם היו מאזור הדרום של ארצות הברית, מה שעזר להעלים בלבול על ידי השפעה גיאוגרפית ותרבותית על הרכב המיקרוביום.
החוקרים חקרו 257 מינים של אורגניזמים במיקרוביום, ומתוכם, הניתוח הצביע על 84 (יותר מ-30%) קשורים למחלת פרקינסון. בסך הכל, ל-36% מהמינים הקשורים ל-PD היה שינוי המשקף עלייה או ירידה של 100-750% אצל PD לעומת קבוצת הביקורת הבריאה.
https://www.uab.edu/news/research/item/13280-new-study-puts-gut-microbiome-at-the-center-of-parkinson-s-disease-pathogenesis - *** תוספת אפריל 24
ניסוי קליני שבוצע בבלגיה מצא שאנשים עם מחלת פרקינסון שקיבלו מנה בודדת של השתלת צואה מתורם בריא, עברו שיפור בתסמינים בהשוואה לאלה שקיבלו פלצבו.
התוצאות, שפורסמו במרץ 24 בכתב העת eClinicalMedicine, העלו כי הציון המוטורי של אנשים שקיבלו השתלת צואה, השתפר ב-5.8 נקודות לאחר 12 חודשים, בהשוואה לשיפור של 2.7 נקודות אצל אנשים שקיבלו השתלת פלצבו. (יאמר לזכות הפלצבו שהוא עושה עבודה טובה גם כן). שיפורים משמעותיים נמצאו גם במדד אובייקטיבי של עצירות (זמן מעבר המעי הגס). - *** תוספת יוני 24
מחקר בראשות חוקרים מבית הספר לרפואה של אוניברסיטת Nagoya שביפן חשף קשר נוסף בין מיקרוביום המעי לפרקינסון. ממצאיהם פורסמו במאי 24 בכתב העת npj parkinson's disease
החוקרים מסבירים שתהליכים פיזיולוגיים שונים מושפעים מאוד ממיקרוביום המעי. בתנאים אידיאליים, הם מייצרים חומצות שומן קצרות שרשקת (SCFAs) ופוליאמינים, השומרים על מחסום המעי המונע כניסת רעלים למחזור הדם. "חדירות גבוהה יותר חושפת את העצבים לרעלנים, תורמת להצטברות לא תקינה של אלפא-סינוקלאין, מפעילה את תאי החיסון במוח ומובילה לדלקת ארוכת טווח", שמשפיעה על תהליכי העברה עצבית שהם קריטיים לשמירה על בריאות הנפש והבריאות הקוגניטיבית.
כדי להבין טוב יותר את הקשר בין המאפיינים המיקרוביאליים של המעי החוקרים ערכו מטאנליזה של דגימות צואה מחולי פרקינסון מיפן, ארצות הברית, גרמניה, סין ו טייוואן. הם השתמשו בטכניקה הנקראת 'ריצוף שוטגאן' שעל פי החוקרים זהו כלי שנותן הבנה טובה יותר של הקהילה המיקרוביאלית והמבנה הגנטי של הדגימה.
הם הבחינו בירידה בגנים החיידקיים האחראים לסינתזה של ריבופלבין (ויטמין B2) וביוטין (ויטמין B7) בחולים שאובחנו עם PD. ריבופלבין וביוטין, המופקים הן ממזון והן ממיקרוביוטה של המעיים, הם בעלי תכונות אנטי דלקתיות, אשר עשויות לנטרל את הדלקת העצבית הנראית במחלות כמו PD.
כדי להבין טוב יותר את הקשר בין המאפיינים המיקרוביאליים של המעי ב-PD, הירושי נישיווקי וג'ון אויאמה מבית הספר לרפואה של אוניברסיטת נאגויה ערכו מטאנליזה של דגימות צואה מחולים עם PD מיפן, ארצות הברית, גרמניה, סין ו טייוואן. הם השתמשו ברצף רובה ציד, טכניקה שמרצפת את כל החומר הגנטי בדגימה. זהו כלי שלא יסולא בפז מכיוון שהוא מציע לחוקרים הבנה טובה יותר של הקהילה המיקרוביאלית והמבנה הגנטי של הדגימה.
הם הבחינו בירידה בגנים החיידקיים האחראים לסינתזה של ריבופלבין (ויטמין B2) וביוטין (ויטמין B7) בחולים שאובחנו עם פרקינסון.
החוקרים מציינים שריבופלבין בבני אדם יכול להגיע מהמזון או מהמיקרוביום. כמו כן מבחינה טיפולית, ריבופלבין משפר עקה חמצונית, תפקוד לקוי של המיטוכונדריה, וויסות דלקת עצבית והפעלה מוגזמת (excitotoxicity) של קולטני חומצות האמינו גלוטמט המתווך מוות נוירוני.
ביוטין גם ידוע כתורם בוויסות דלקת, משפר פגמים מוטוריים ואופטיים.
החוקרים חושבים ש"תיסוף המתמקד בריבופלבין וביוטין מהווה דרך טיפולית פוטנציאלית להקלה על תסמיני PD ולהאטת התקדמות המחלה.
https://www.nagoya-u.ac.jp/researchinfo/result-en/2024/06/20240618-01.html - סקירה שפורסמה ביולי 24 בכתב העת Chemical Research in Toxicology בוחנת כיצד חומרי הדברה וחיידקי מעיים משפיעים בנפרד על התפתחות והתקדמות PD, תוך הדגשת ההשפעות המזיקות של חומרי הדברה ושינויים בחיידקי המעי. הצוות הסיק שחשיפה לחומרי הדברה קשורה להופעת PD באמצעות "הפרעות בתפקוד המעי ושינויים במיקרוביוטה של המעיים". המחקר גם מצביע על עלייה בנוכחות ובירידה של משפחות וסוגים חיידקיים ספציפיים בחולי PD בהשוואה לאלו שללא. בנוסף, הסקירה מרכיבה רשימה של שפע דיפרנציאלי של חיידקי מעיים הקשורים לתסמינים לא מוטוריים ומוטוריים בחולי PD, שכן כל שלב של המחלה עשוי להיות במתאם עם פרופיל חיידקי מסוים.
הצוות מדווח שמספר מחקרים מראים שינויים בהרכב חיידקי המעי ו"שינויים לאחר מכן במוצרים ובמטבוליטים בחולי PD". הסקירה חושפת הבדלים ב-53 משפחות מיקרוביאליות ו-98 סוגים בין אנשים עם PD לאלו שאין להם.
הסקירה גם מדגישה מספר מחקרים המדווחים על שינויים בשפע של משפחות חיידקי מעיים וסוגים ספציפיים בחשיפה לחומרי הדברה שונים. למשל שחומרי הדברה ושינויים בקהילה המיקרוביאלית משבשים את מחסום המעי, ובכך גורמים לדלקת ולהצטברות אלפא-סינוקלאין (a-syn) שעלולים לשבש את מערכת העצבים ולהוביל להצטברות חריגה של חלבוני a-syn שיכולים להתפזר לאזורי מוח שונים דרך עצב הוואגוס. - מחקר שפורסם במאי 25 בכתב העת Frontiers and Nutrition בחן את הקשר בין צריכת חיידקים חיים בתזונה לבין שכיחות מחלת פרקינסון (PD) בקרב מבוגרים מעל גיל 40.
מזונות מסווגים לשלוש דרגות על סמך תכולת החיידקים החיים: נמוכה (מזונות שעברו פיסטור או עיבוד בטמפרטורות גבוהות), בינונית (ירקות ופירות טריים לא קלופים) וגבוהה (מזונות מותססים לא מפוסטרים ותוספי פרוביוטיקה).
סך של 26,033 נבדקים נכללו במחקר זה, שכללו 314 חולים עם PD, שחולקו לשלוש קבוצות על סמך צריכת מזונות עם רמות שונות של תוכן מיקרוביאלי: גבוהה (20.1%), בינונית (45.4%) ונמוכה (34.5%).
ניתוח רגרסיה לוגיסטית רב משתנית גילה כי נבדקים עם הצריכה הגבוהה והבינונית של חיידקים חיים מהתזונה מפגינים שכיחות מופחתת של 48%- ו-27%- למחלת פרקינסון בהשוואה לאלו עם צריכה נמוכה. ניתוח נוסף הצביע על קשר ליניארי משמעותי בין צריכת חיידקים חיים מהתזונה לבין שכיחות מחלת פרקינסון. - *** תוספת אוקטובר 25: מדד DI-GM
מחקר עוקבה רוחבי רחב היקף, שפורסם באוקטובר 25 בכתב העת Nutrition Journal, מחזק באופן משמעותי את התפיסה כי תזונה הממוקדת בבריאות המיקרוביום מהווה כלי קריטי במניעת מחלת פרקינסון (PD). המחקר, שהתבסס על נתוני סקר NHANES מקיף של 17,373 משתתפים בני 40 ומעלה, ביקש לבחון את הקשר בין ציון המדד התזונתי למיקרוביוטת המעיים (DI-GM) לבין שכיחות PD. מדד DI-GM הוא כלי חדש המעריך באופן מקיף 14 רכיבי מזון, הכוללים מרכיבים המשפרים את הרכב המיקרוביום ומרכיבים שאינם משפרים או משנים לרעה את הרכבו.
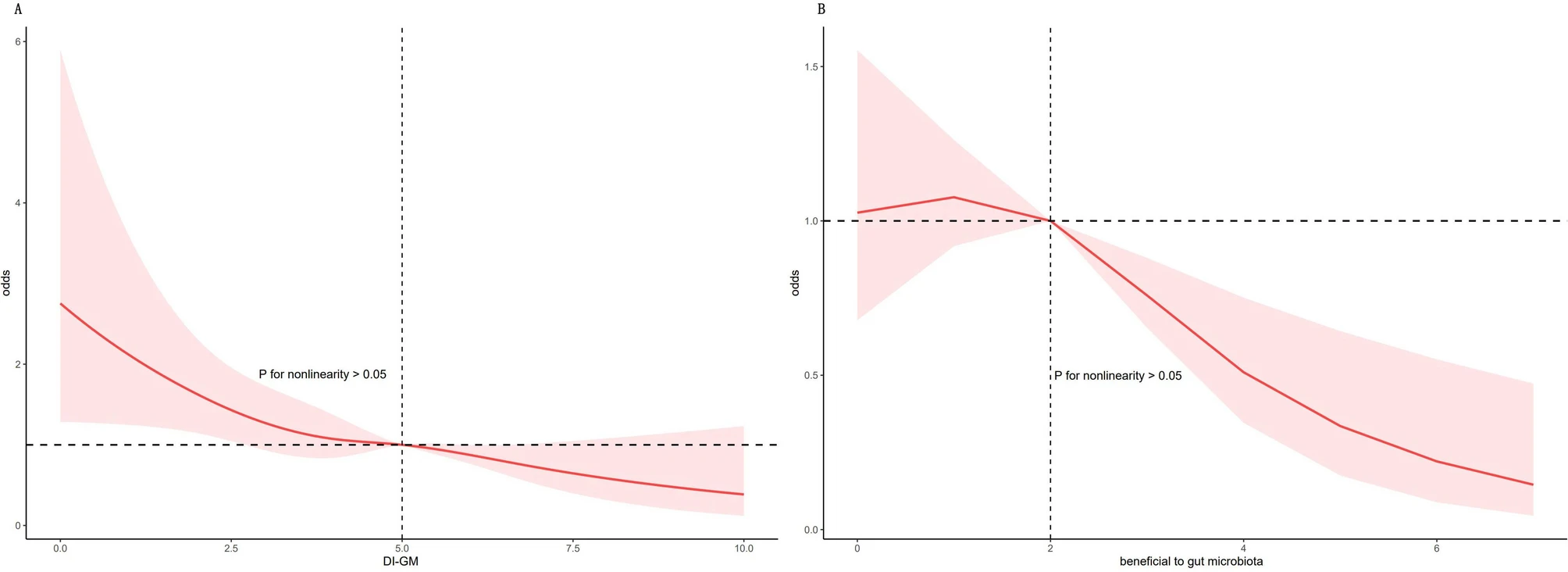
המחקר אישר את ההשערה: אנשים בעלי ציון DI-GM גבוה יותר, המעיד על תזונה התומכת בייצור SCFAs (חומצות שומן קצרות שרשרת) ובתמיכה עצבית, הראו הפחתה משמעותית בשכיחות PD. הנתונים הראו כי אלו שציונם במדד היה גבוה (≥6) נמצאו עם 49% פחות סיכון לשכיחות PD, בהשוואה לאלו עם ציונים נמוכים יותר. הקשר הלא לינארי שנמצא מראה שההגנה גוברת משמעותית ככל שאיכות התזונה עולה.
__ __
__
בעוד שהחוקרים הדגישו כי כבר בציון DI-GM≥6 מושגת הפחתה מובהקת של 49% בשכיחות PD (הסף הקליני המעשי), על פי ניתוח הגרף המציג את הקשר הרציף (מודל RCS) מגלה כי היתרון ממשיך לגדול משמעותית ככל שהציון עולה. השאיפה לדיאטה מיטבית המגיעה לציון 10 מביאה להפחתה משוערת של כ-65% בסיכויים לשכיחות PD, מה שמדגיש את היתרון שבאימוץ אורח חיים מיטבי.
ממצאים אלו מחזקים את המנגנון המוכר של ציר המעי-מוח, ומצביעים על כך שתזונה מעודדת מיקרוביום מפחיתה את הדלקת המערכתית ומעלה את ייצור המטאבוליטים המגנים, ובכך תורמת להגנה מפני התפתחות PD והצטברות חלבון ה-α-synuclein.
מחקר זה מספק אישור קליני רב-עוצמה למסקנות הקודמות שלעיל בדבר חשיבות המיקרוביום והאסטרטגיה התזונתית. הוא מעגן את הראיות הקודמות על חשיבות הסיבים, העמילנים העמידים והפוליפנולים, בכך שהוא מציג מדד תזונתי מקיף שמעמיד את בריאות המיקרוביום במרכז ההגנה הנוירולוגית. הקשר המגן שנמצא היה יציב ונשמר בכלל הקבוצות הדמוגרפיות ואף לאחר ניכוי גורמי סיכון נפוצים כגון סוכרת ומחלות לב.
DI-GM הוא מדד חדש המשקף את מגוון מיקרוביום המעי בהקשר של מזונות. כלומר מבטא את הקשר בין מזונות או קבוצות מזון לאופי מיקרוביום המעי.
מדד זה מסוכם במונחים של ראיות להשפעה מועילה, שלילית או ללא השפעה נצפית, על מדדי גיוון חיידקי ( α ו-β), רמות חומצות שומן קצרות שרשרת (בוטיראט, אצטט, פרופיונאט, איזובוטיראט – SCFA) בצואה ושינוי ביחסי המערכות וחיידקים ספציפיים.
כאשר רכיבים מיטיבים כוללים: חומוס, סויה, דגנים מלאים, סיבים תזונתיים, חמוציות, אבוקדו, ברוקולי, מוצרי חלב מותססים, קפה ותה ירוק.
רכיבים שליליים כוללים: דגנים מזוקקים, בשר אדום, בשר מעובד ויותר מ-40% מהאנרגיה היומית משומן רווי וטרנס.
השפעה מיטיבה הוגדרה כעלייה ב:
Faecalibacterium, Bifidobacterium, Lactobacillus, Lactococcus, Parabacteroides, Roseburia,
Eubacterium rectale, Eubacterium hallii, Akkermansia, Prevotella, Prevotella copri, Anaerostipes, Anaerostipes hadrus, Veillonellaceae, Parabacteroides distasonis, Gemmiger, ו- Moraxellaceae .
וירידה ב:
Bacteroides, Bacteroides fragilis, Fusobacteria, Streptococcus, Clostridium, Clostridium symbiosum, Clostridium perfringens, Dialister, Alistipes, Bilophila, Ruminococcus gnavus, Dorea, Actinomyces, Odoribacter, Blautia, Lachnospira, Lachnospiraceae, Sutterella, Enterobacteriaceae, ו- Klebsiella sp.
המדד כולל בתוכו שיטת ניקוד כאשר על כל מזון חיובי שנצרך מעל החציון של משתתפי המחקר מקבלים נקודה. ולהיפך, על כל מזון שלילי שנצרך מתחת לחציון של משתתפי המחקר מקבלים נקודה.
הציונים הללו מחולקים בדרך כלל לקבוצות (לדוגמה: 0-3 נקודות, 4 נקודות, 5 נקודות, ו-6 נקודות ומעלה).
המסקנה המתבקשת היא: כל אחד אמור לדאוג למיקרוביום שלו. בהגנה עליו ובטיפוח שלו.
איך שומרים על מיקרוביום מגוון ובריא?
תזונה מגוונת מבוססת צומח[1] (כל הצבעים, כל הטעמים, כל המרקמים), כל המשפחות (פירות וירקות עם קליפה, דגנים מלאים, קטניות, אגוזים, שקדים, זרעים ונבטים ומונבטים) וגם בתוך המשפחות לגוון לדוגמה: ירוקים זה לא רק חסה ופטרוזיליה. זה גם מנגולד, רוקט, רוקולה, תרד, סלרי, בזיליקום, נענע ועוד ועוד. עדשים זה גם ירוק, צהוב, כתום, חום, שחור, קטניות יש עשרות סוגים. כאשר יש סייג אחד. מה שלא עושה טוב. מורידים!
דרכים נוספות לקבל לחיזוק החיידקים הטובים: סיבים תזונתיים, עמילנים עמידים ומזון מותסס: כרוב כבוש (sauerkraut)[1], קימצ'י (קוראני), טמפה (אינדונזי), נאטו ומיסו (יפני), משקה קומבוצ'ה. וכמובן התססת פירות וירקות ביתית. והמדריך הבא לדעתי הוא השלם ביותר חלק 1, חלק 2. ישנה גם הדרכה דרך סרטונים אחרי הרשמה כאן.
במקביל להמנע ממגע וצריכה של:
תרופות המשנות לרעה את הרכב המיקרוביום במיוחד אנטיביוטיקה, אבל גם נוגדות חומציות (PPI), מטפורמין, לקסטיבים, תרופות נוגדות דיכאון (SSRI), סטרואידים ונוגדי דלקת שאינם סטרואידים.
חומרי חיטוי (אנטיבקטריאליים) המכילים למשל טריקלוזן.
תכשירים המכילים משבשי אותות אנדוקריניים כגון פתלאטים ו'חומרים אורגניים מופלרים, PFAS, BPA, מעכבי בעירה, מזונות מרוססים[2][3] ואולי במיוחד גלייפוסט. וגם פלסטיק.
מזון מעובד[2][3][4][5]/ ומזון מסוכר.
החלק של תזונה: בריא מול לא בריא
*** תוספת נובמבר 25
סקירת מטא-אנליזה מקיפה של מחקרי עוקבה פרוספקטיביים, אשר פורסמה בנובמבר 25 בכתב העת Nutrition Reviews מנתחת את הקשר בין צריכת קבוצות מזון שונות לבין הסיכון למחלת פרקינסון (PD).
מחקר זה, שכלל ניתוח של 29 מחקרים עם למעלה מ-1.3 מיליון משתתפים, נועד לזהות דפוסים ומרכיבי מזון המגבירים או מפחיתים באופן מובהק את הסיכון למחלה.
החוקרים מצאו אישור חזק לעקרונות המנחים: דבקות בדפוסי תזונה בריאים הייתה קשורה להפחתה משמעותית של 37% בסיכון ל-PD, בעוד שדבקות בדפוסי תזונה לא בריאים נקשרה לעלייה של 40% בסיכון, ובכך מחזקת את הקשר הברור בין איכות התזונה למצב הנוירולוגי.
הניתוח גם חשף דיוק הכרחי להנחיות הקשורות למוצרי חלב שלעתים נכללים בתזונה "בריאה", שכן צריכה גבוהה שלהם נמצאה קשורה לעליה ישירה בסיכון לפרקינסון בקשר של מנה-תגובה. הנתונים הסטטיסטיים הראו כי צריכה גבוהה של מוצרי חלב הייתה קשורה לעלייה של 26% בסיכון ל-PD, כאשר צריכת מוצרי חלב דלי שומן הייתה קשורה לעלייה גבוהה אף יותר של 30% בהשוואה לקטגוריית הצריכה הנמוכה ביותר. ניתוח ליניארי הדגים עלייה של 13% בסיכון ל-PD לכל כוס חלב שנצרכה ביום, ועלייה של 4% לכל 10 גרם גבינה ביום. ניתוח תת-קבוצתי אף גילה כי קשר שלילי זה היה חזק יותר באופן עקבי בקרב גברים.
במקביל, מתוך כל קבוצות המזון שנבדקו, קבוצה אחת בלטה בהגנה נוירולוגית ממוקדת: קטניות ואגוזים היו קבוצת המזון היחידה שהראתה הפחתה מובהקת של 29% בסיכון ל-PD. מסקנת החוקרים היא כי למרות היתרונות של דפוס תזונה בריא כללי, חיוני להתמקד בהגבלה של מוצרי חלב, ובמקביל לעודד צריכה גבוהה של קטניות ואגוזים, למען מניעה יעילה.
ממצאי המטא-אנליזה מעניקים אישור קליני מכריע ומתחברים ישירות לליבת המאמר הנוכחי. הקשר החיובי החזק בין דפוסי תזונה בריאים (דוגמת אלו המשקפים את מדד ה-DI-GM) לבין הפחתת הסיכון ל-PD, מאשש את חשיבותו של מיקרוביום מאוזן.
כמו כן הניגוד הדרמטי שנמצא במוצרי חלב מחזק את הטיעון המרכזי בדבר גורמים סביבתיים וכימיקלים המתווכים את המחלה דרך המעי שכן חוקרים משערים כי העלייה בסיכון נובעת מחשיפה כרונית לרעלנים מסיסים בשומן (כמו שאריות חומרי הדברה) המצטברים בחלב, וכן מהפחתה ברמת חומצת השתן המהווה מגן נוירולוגי חיוני למוח. בכך מדגישה את הצורך בהנחיות תזונתיות מדויקות המשלבות תמיכה במיקרוביום עם הגבלה ספציפית של מרכיבים שחושפים את מערכת העצבים לרעלים.
*** תוספת דצמבר 25 – ויטמינים, שומנים ודפוסי תזונה במניעת פרקינסון
מחקר סקירה נרחב שפורסם בדצמבר 25 בכתב העת Frontiers in Nutrition ביקש לבחון לעומק את תפקידם של רכיבי תזונה פעילים במניעה ובעיכוב של מחלת הפרקינסון (PD), זאת לאור העלייה העולמית בשכיחות המחלה והצורך באסטרטגיות שאינן רק תרופתיות. הסקירה, שכללה ניתוח של למעלה מ-20 מחקרים תצפיתיים וקליניים לצד מודלים בבעלי חיים, התמקדה במדדים של הישרדות נוירונים דופמינרגיים (תאי העצב המייצרים דופמין) והצטברות חלבון ה-אלפא-סינוקלאין, המהווה את הסימן הפתולוגי המרכזי למחלה.
החוקרים מצאו כי ויטמין D3 פועל כרכיב נוירו-פרוטקטיבי (מגן עצבי) קריטי, שכן הוא מעורר את הביטוי של אנזים הכרחי בסינתזת דופמין (Tyrosine hydroxylase), וכי רמות נמוכות של הוויטמין בדם היו נפוצות משמעותית בקרב חולי פרקינסון לעומת קבוצות ביקורת בריאות.
במקביל, המחקר הדגיש את החשיבות המכרעת של חומצות שומן רב-בלתי רוויות (PUFAs). נמצא כי בקרב חולים קיימת ירידה משמעותית ברמות ה-DHA (אומגה 3) וה-AA (חומצה ארכידונית, אומגה 6), בעוד שרמות השומן הרווי (SFA) היו גבוהות בכמעט מחצית; החוקרים מצאו כי תיקון מאזן זה, בדגש על הגברת חומצות שומן מסוג אומגה 3, הראה יכולת להפחית את העקה החמצונית במוח ולשפר באופן מובהק את התפקוד המוטורי.
ממצא מרכזי נוסף בסקירה זיהה ארבע קבוצות פוליפנולים כעמודי התווך של ההגנה העצבית הישירה: פלבנואידים (פירות יער ותה), חומצות פנוליות, סטילבנים (כמו רזברטרול מענבים) וליגנאנים (שומשום ופשתן). רכיבים אלו פועלים כ"סלקטורים" המונעים מחלבון האלפא-סינוקלאין להתגבש למשקעים רעילים.
ממצאי המחקר התרחבו גם לבחינת דפוסי תזונה שלמים. שם נמצא כי דפוס ה-MIND (שילוב בין תזונה ים-תיכונית לתזונה למניעת יתר לחץ דם) הוא המשמעותי ביותר למניעה, כאשר כל עלייה של נקודה אחת במדד הדבקות בדיאטה נמצאה כקשורה להפחתה של 13% בסיכון ללקות במחלה. במקביל, המחקר הציג ממצאים לגבי התזונה הקטוגנית (KD), אשר הראתה יכולת לשפר תפקוד קוגניטיבי ותסמינים מוטוריים דרך אספקת גופי קיטון כדלק חלופי למוח.
עם זאת, בפרקים העוסקים במנגנונים הביולוגיים של המחלה, המחקר קבע כי צריכה גבוהה של שומן רווי (SFA) ומחסור בסיבים תזונתיים – המאפיינים תפריטים דלי פחמימות מסוימים – מעודדים דלקת עצבית ופוגעים בייצור ה-SCFAs במעי. (*** החוקרים לא מציינים את הסתירה הזו בין התועלת המטבולית של הקיטו לבין הנזק הדלקתי הפוטנציאלי מרכיביה (שומן רווי ומחסור בסיבים), אך הצלבת הממצאים בתוך הסקירה מעלה כי מדובר בדילמה קלינית משמעותית בניהול המחלה***)
כמו כן התזונה המערבית המאופיינת ב"שלושת הגבוהים" (קלוריות, חלבון ושומן רווי) נמצאה כמעודדת דלקת עצבית דרך ציר המעי-מוח (Gut-Brain axis), המקשר בין חוסר איזון בחיידקי המעי לבין פגיעה בתפקוד המוחי.
החוקרים גם הדגישו בדיון כי ויטמין C ו-E פועלים כנוגדי חמצון המונעים את התגבשותו הרעילה של האלפא-סינוקלאין בקרב חולים מבוגרים.
ממצאים אלו מעניקים אישור קליני רב-עוצמה לראיות הקודמות בדבר מרכזיוּת המיקרוביום והתזונה בניהול מחלת הפרקינסון. בעוד שמידע קודם התמקד בעיקר בהשפעות הרעילות של חומרי הדברה על המעי, המחקר הנוכחי סוגר את המעגל המדעי ומראה כיצד רכיבים תזונתיים ספציפיים כמו הפלבנואידים והליגנאנים יכולים לנטרל את אותה רעילות ברמה התאית. האינטגרציה בין המיקרוביום המייצר SCFAs לבין צריכה של פוליפנולים, ויטמינים וחומצות שומן רב-בלתי רוויות מהצומח, יוצרת סינרגיה המגנה על שלמות המיטוכונדריה ומחסום הדם-מוח. מחקר זה מאשש כי האסטרטגיה היעילה ביותר למניעת המחלה ועיכובה טמונה באימוץ תפריט צמחי עשיר בסיבים ודל בשומן רווי, המזין את חיידקי המעי המועילים ובכך מונע את נדידת התהליכים הדלקתיים מהמעי אל מערכת העצבים המרכזית.
החלק של מזון מעובד (סעיף 6)
שימו לב מה מצאו לגבי תרופה נפוצה לפרקינסון
במחקר שפורסם בנובמבר 24 בכתב העת Nature Microbiology בהובלת מדענים מאוניברסיטת וינה, ובשיתוף אוניברסיטאות סאות'המפטון, אלבורג ובוסטון, נחשף כי תרופת אנטקפון שנרשמת באופן נרחב למחלת פרקינסון (בשילוב עם לבדופה) משבשת באופן משמעותי את המיקרוביום של המעי האנושי על ידי גרימת מחסור בברזל. המחקר מספק תובנות חדשות לגבי ההשפעה שלעתים קרובות מתעלמים ממנה, על הקהילות המיקרוביאליות הממלאות תפקיד קריטי בבריאות האדם. ועוד המחלות שהקשר למיקרוביום הוא עצום.
החוקרים מציינים שעד כה, רוב המחקרים שחקרו את האינטראקציות בין תרופות למיקרוביום הסתמכו או על ניתוחי עוקבה של חולים שהושפעו מגורמים מבלבלים רבים או על ניסויים באמצעות חיידקי מעיים מבודדים, שאינם קולטים במלואם את המורכבות של המיקרוביום האנושי.
לכן במחקר הנוכחי המדענים השתמשו בגישה חדשה, הם חקרו את ההשפעות של חשיפת שתי תרופות – אנטקפון ולוקספין (תרופה לסכיזופרניה) על דגימות צואה מתורמים אנושיים בריאים. ולאחר מכן ניתחו את ההשפעה על הקהילות המיקרוביאליות באמצעות טכניקות מולקולריות והדמיות מתקדמות. הצוות גילה שלוקספין ועוד יותר אנטקפון עיכבו קשות חברי מיקרוביום מועילים רבים, בעוד אחרים כמו E-coli שגשגו באופן חריג.
החוקרים שיערו ש'אנטקפון' עלול להפריע לזמינות הברזל במעיים, משאב חיוני עבור חיידקים רבים. הניסויים שלהם אישרו שהוספת ברזל לדגימות צואה המכילות אנטקפון מונעת את השפעותיה של התרופה שמשנות את המיקרוביום. חקירה נוספת העלתה כי E. coli, ששגשג בתנאים אלו, נושא מערכת ספיגת ברזל יעילה ביותר מה שאפשר להם להתגבר על הרעבת הברזל ולהתרבות, גם בנוכחות התרופה.
כלומר המנגנון הוא: תרופה שגורמת למחסור בברזל ולשגשוג חיידקים שמתאימים יותר למצב של מחסור ברזל.
החוקרים מציינים שללגילוי זה יש השלכות רחבות יותר על ההבנה כיצד תרופות אחרות עשויות להשפיע על המיקרוביום של המעי. מספר תרופות, כולל 'אנטקפון', מכילות קבוצות קטכול קושרות מתכת, מה שמצביע על כך שמנגנון זה יכול להיות מסלול נפוץ יותר לשינויים במיקרוביום הנגרמות על ידי תרופות, חומרי הדברה ותוספי מזון (E-Mumbers), שכן קטכול הוא חומר גלם בייצור אלה.
מבחינת החוקרים הממצאים מציגים גם הזדמנות למתן את תופעות הלוואי של תרופות כמו אנטקפון. על ידי הבטחת זמינות מספקת של ברזל למעי הגס, ייתכן שיפחית את הדיסביוזה ואת בעיות מערכת העיכול הנלוות לעיתים קרובות.
מכיוון שהם שבויים בקונספט הרפואה הפרמצבטית. השלב הבא שלהם יהיה לחקור כיצד לתמוך טוב יותר במיקרוביום המעי כגון אספקת ברזל באופן סלקטיבי למעי הגס, שם זה יכול להועיל למיקרוביום מבלי להפריע לספיגת התרופה במעי הדק. *** כלומר לא לשנות חלילה. אלא להוסיף.
https://medienportal.univie.ac.at/en/parkinsons-drug-changes-the-gut-microbiome-for-the-worse-due-to-iron-deficiency
דברים נוספים (שלא הוזכרו למעלה) שנמצאו מועילים לפרקינסון:
- שיפור תפקודי המיטוכונדריה היא אולי הדרך למנוע הצטברות פלאקים חלבוניים רעילים במוח – אורוליטין A מטבוליט טבעי שנוצר על ידי חיידקי מעי טובים, כאשר אנו אוכלים רימונים, פירות יער ואגוזים שמכילים אלגיטאנינים (ellagitannins).
- פלבנואידים.
- סולפוראפן (מצליבים) סעיף 3.2.2.
- משקה נוני.
- מאש.
- ססמינול הנמצא בקליפת השומשום מונע פרקינסון.
- ויטמין די
- סקירה שפורסמה ב-2012 סיכמה את העדויות לגבי תפקידו של ויטמין D בפרקינסון, כולל היבטים נוירו-הגנתיים והתפקיד של קולטני ויטמין די (VDR) במוח. היא מדגישה את הקשר בין חסר ויטמין D למחלה ואת הפוטנציאל לשיפור התוצאות באמצעות ויטמין D.
- מחקר סקירה ומטא אנליזה מ-2019 מצא קשר הפוך מובהק בין רמות ויטמין D לבין סיכון לפרקינסון, וגם קשר הפוך מובהק בין רמות ויטמין D לבין חומרת התסמינים המוטוריים בפרקינסון. כלומר, רמות נמוכות יותר של ויטמין D היו קשורות לסיכון גבוה יותר למחלה ולתסמינים מוטוריים חמורים יותר.
- סקירה מ-2020 תומכת גם בהיבטים הנוירו-הגנתיים של ויטמין די.
- בסקירה מ-2022 דנו כיצד רמות ויטמין D בסרום קשורות לתסמיני מחלת פרקינסון ולהתקדמות קלינית, ובשימוש האפשרי בו על מנת לשפר את הביטוי הקליני בחולים עם מחלת פרקינסון.
- מחקר מטא-אנליזה שפורסם ביוני 25 בכתב העת Frontiers in Nutrition, סקר נתונים מ-8 ניסויים אקראיים מבוקרים שכללו 646 חולי פרקינסון. מטרת המחקר הייתה להעריך את השפעת תוספי ויטמין D על תסמינים מוטוריים במחלה. המחקר בחן מספר מדדים עיקריים לתפקוד המוטורי: סולם דירוג מחלת פרקינסון המאוחד (UPDRS III) להערכה קלינית מקיפה של חומרת המחלה, מבחן "קום ולך" (TUG) ומבחן הליכה 10/8 מטר להערכת ניידות ושיווי משקל, ומבחן הליכה 6 דקות להערכת סיבולת. למרות שלא נמצא שיפור מובהק בכלל המדדים המוטוריים, הממצא החיובי והבולט ביותר הצביע על כך שתוסף ויטמין D האריך באופן משמעותי את מרחק ההליכה במבחן 6 דקות (בממוצע של 24.85 מטרים נוספים). משמעות הדבר עבור חולי פרקינסון היא שיפור פוטנציאלי בניידות התפקודית, סיבולת ההליכה ואיכות החיים ביומיום, גם אם הוא אינו משפיע על כל היבטי המחלה. המאמר מסכם כי ויטמין D עשוי למלא תפקיד מעכב פעיל במנגנוני התפתחות הפרקינסון, ומספק המלצות לטיפול תומך זה.
- ויטמין K2 מתקן תאי עצב באמצעות לולאת בקרת איכות מיטוכונדריאלית.
- הקשר בין אבץ לפרקינסון.
- *** תוספת פברואר 26 – חומצה פנטוטנית (ויטמין B5)
סקירה סיסטמית ומטבולומית מקיפה, אשר פורסמה בפברואר 26 בכתב העת Nutrition Reviews, שופכת אור חדש על הקשר שבין ויטמינים מקבוצת B לבין התפתחות מחלת הפרקינסון (PD), תוך התמקדות בחומצה פנטוטנית (ויטמין B5). החוקרים ביקשו לבחון האם מצב תת-אופטימלי של ויטמין זה, המהווה רכיב ליבה בייצור של קו-אנזים A (CoA), מהווה גורם מפתח בהידרדרות של תאי העצב מייצרי הדופמין. הסקירה ניתחה 19 מחקרים שכללו הערכות תזונתיות לצד ניתוחים מטבולומיים (בדיקת תוצרי חילוף חומרים) מתקדמים של נוזלי גוף, מבני מוח ודגימות צואה של חולים לעומת בריאים.
הממצאים המדעיים מצביעים על קשר הפוך מובהק: צריכה תזונתית גבוהה של חומצה פנטוטנית נמצאה קשורה לירידה משמעותית בסיכון לפתח את המחלה. במישור המטבולי, ב-16 מחקרים שונים, זוהתה החומצה הפנטוטנית כחומר שרמתו משובשת אצל חולים באופן עקבי; ברוב המוחלט של המקרים (12 מתוך 16 מחקרים), נמצאו רמות נמוכות משמעותית של הוויטמין אצל חולי פרקינסון בהשוואה לקבוצות ביקורת בריאות. מעבר לכך, החוקרים זיהו כי שיבושים במסלול הייצור של חומצה פנטוטנית לקו-אנזים A עשויים לשמש ככלי אבחנתי יעיל להבדלה בין חולים לבריאים. מסקנת החוקרים היא כי חוסר זמינות של ויטמין B5 או הפרעה בעיבודו בגוף פוגעים ביכולת של תחנות הכוח בתא (המיטוכונדריה) לייצר אנרגיה ותורמים באופן ישיר למות תאים במערכת העצבים המרכזית.
ממצאי המחקר מעניקים אישור קליני מכריע לראיות הקודמות בדבר מרכזיותה של המיטוכונדריה בניהול מחלת הפרקינסון ומראה כיצד ויטמין B5 מהווה חוליה חסרה והכרחית לתחזוקת ה-CoA, שבלעדיו תהליכי הניקוי והשיקום של התא אינם יכולים להתבצע ביעילות. האינטגרציה בין המיקרוביום, המושפע מחומרי הדברה וזקוק להזנה נכונה, לבין זמינות של חומצה פנטוטנית מהצומח, יוצרת מעטפת הגנה כפולה: מניעת הצטברות רעילה של חלבוני אלפא-סינוקלאין על ידי פוליפנולים, והבטחת האנרגיה התאית הדרושה לפינויים מהמוח. ממצאים אלו מאששים כי האסטרטגיה היעילה ביותר למניעת המחלה ועיכובה מחייבת דגש על צפיפות רכיבי תזונה גבוהה הכוללת מקורות עשירים ל-B5, התומכים בתפקוד האנרגטי של התא ומסייעים בתיקון הנזקים הנגרמים מחשיפות למזהמים סביבתיים. - צמחים ונוטרינטים שהוזכרו בבלוק הניקוי למעלה (עם לינקים) – אומגה 3, אשווגנדה, זעפרן, אסטקסנטין, רימונים, כורכום, ג'ינג'ר, גדילן, רזברטרול, קוורצטין.
- פעילות גופנית [1].
לחלק של הפרקטיקה! מה עושים עכשיו ואיך מיישמים את כל הידע הזה.
🧰 ארגז הכלים המעשי, 🗓️ תוכניות פעולה הדרגתיות ליישום הרגלים קריטיים.
🛒 רשימות קניות ממוקדות וטבלאות רכיבים, 👨🍳 מתכונים קלים ומדויקים.
💡 הנחיות יישום (מה זה אומר בפועל). 🔬 הרחבות, נספחים, 🚨 תוספים ודיוקים.
🌟המודולים מסודרים בטבלה לפי נושאים נחקרים 🌟
👈 מוזמנים לפנות אלי באופן פרטי לווטסאפ (0544-606696).👉
🤝 ולהכיר את הקבוצה: "לצאת מעדר הרגיל – הפרקטיקה"
היי לך.. אני משקיע שעות רבות כל יום באיתור ותרגום מאמרים כדי לספק לכולם את המידע העדכני ביותר, לבריאות טובה בדרך הטבע. וכדי שאוכל להמשיך לספק את המידע ולתחזק את האתר. כל תרומה, גדולה או קטנה תהיה לעזר רב. לתרומה נוחה ופשוטה דרך Pay Pal.
מוזמנים להזין דוא"ל למטה כדי להתעדכן ראשונים





כתיבת תגובה